서 언
재료 및 방법
실험재료
1-MCP 처리 및 저장조건
과실 특성 조사
세포벽물질(Alcohol Insoluble Substance, AIS) 추출
Uronic Acid 및 Total Sugar 함량
세포벽분해효소 추출
세포벽분해효소 활성 측정
통계분석
결과 및 고찰
수확시 과실 특성
저장기간동안 과실 특성
Total Sugar(TS)와 Uronic Acid(UA)의 함량
세포벽분해효소 활성 변화
상관관계 분석
서 언
2019년 국내 사과(Malus domestica Borkh.) 재배면적은 32,954ha으로 증가하고 있는 추세이고(Statistics Korea, 2019), 최근 농촌진흥청 국립원예특작과학원에서는 ‘후지’ 사과 중심의 재배체계에서 벗어나 재배 품종의 다양화를 위하여 조생종 신품종이 육성되고 있다. 그동안 대표적인 조생종인 ‘쓰가루’ 사과는 오랜 기간 소비자로부터 호평을 받아왔지만 수확 전 낙과와 저장성이 약하여 과실 품질이 빠르게 저하된다는 단점이 지적되어 왔다(Park et al., 2000). 따라서 국립원예특작과학원에서는 이러한 ‘쓰가루’ 사과를 대체하기 위하여 ‘썸머프린스’와 ‘썸머킹’ 사과를 육성하였다. ‘썸머프린스’ 사과는 ‘쓰가루’에 ‘OBIR2T47’을 교배하여 2014년 최종 선발된 품종으로 숙기는 7월 하순, 과중은 290g, 경도는 3.1kg(/∮8mm), 가용성 고형물 함량은 12.1°Brix, 산 함량은 0.54%로 산미가 비교적 높은 품종이다. ‘썸머킹’ 사과는 ‘후지’에 ‘골든델리셔스’를 교배하여 2010년 최종 선발된 품종으로, 숙기는 8월 상순, 과중은 265g, 경도는 3.7kg(/∮8mm), 가용성 고형물 함량은 13.9°Brix, 산 함량은 0.43%로 같은 시기에 재배되는 조생종 사과와 비교하여 식미가 뛰어나다고 평가받고 있다(Kwon et al., 2011; Yoo et al., 2016). 그러나 최근 국내 사과 소비 트렌드는 다양한 사과 품종들의 연중 소비가 요구되고 있지만 이들 품종은 단기간 저장 및 유통되고 있는 실정으로 소비자의 기대에 미치지 못하고 있는 실정이다.
사과는 대표적인 호흡급등형 과실로서 저장기간동안 호흡 급등과 함께 에틸렌 발생량이 증가하게 되고(Johnston et al., 2001; Kwon et al., 2017), 이는 저장성과 상품성을 저하시키는 원인이 된다(Yang et al., 2013; Park et al., 2016; Kim et al., 2018; Win et al., 2019; Yoo et al., 2019). 그동안 저장중 과실의 연화현상을 억제하기 위하여 1-methylcyclopropene (1-MCP)를 적용하여 왔고, 그 결과 사과 과실의 에틸렌 생성과 호흡률 감소, 경도와 산 함량 유지, 노화와 관련된 저장장해의 발생 경감 등 우수한 효과를 나타내고 있다(Fan et al., 1999a, 1999b; DeEll et al., 2007; Watkins, 2007; Win at al., 2019). 1-MCP 처리방법은 수확 후 7일 이내에 1µL·L-1의 농도로 24시간 동안 밀폐된 공간에서 훈증처리 하였을 때 최상의 효율을 보인다고 하였으며(AgroFresh, 2014; DeEll et al., 2016), ‘McIntosh’ 사과와 같이 높은 에틸렌 발생량을 보이는 경우 수확 후 3일 이내 처리하는 것이 효과적이라고 하였다(DeEll et al., 2008). 캐나다의 경우 과실의 수확과 저장환경을 고려하여 1-MCP를 1µL·L-1의 농도로 수확 후 240일 내에 최대 4회까지 처리한다고 하였다(DeEll et al., 2016). 그러나 국내에서는 모든 과실에 1-MCP를 1µL·L-1의 농도로 1회 처리만을 실시하고 있어 1-MCP 처리 농도 및 횟수에 대한 연구는 없는 실정이다.
따라서 본 연구에서는 국내 육성 조생종인 ‘썸머프린스’와 ‘썸머킹’ 사과에 1-MCP 처리 농도와 횟수에 따른 저온저장 중 과실 품질과 세포벽 대사에 미치는 영향을 분석하여 효과적인 1-MCP 적용 방법을 구명하고자 하였다.
재료 및 방법
실험재료
본 실험은 2018년 경북 군위군에 위치한 국립원예특작과학원 사과연구소에 재식되어 있는 ‘썸머프린스/M.9’(5년생)와 경북 문경시농업기술센터 사과연구소에 재식되어 있는 ‘썸머킹/M.9’(6년생) 품종의 수세가 안정된 나무에서 각각 7월 23일과 8월 6일에 수확한 과실을 재료로 수행되었다. 수확 후 외형적으로 건전하며 성숙 정도가 고른 과실을 선별하여 실험에 사용하였다.
1-MCP 처리 및 저장조건
처리 약제는 1-MCP(3.3%, 상품명: SmartFreshTM, AgroFresh, Yakima, WA, USA)로, 수확 직후 과실을 밀폐된 공간에 두고 각각 0.5µL·L-1 및 1µL·L-1의 농도로 상온에서 18시간 훈증 처리한 후 저장고에 입고한 것을 1회 처리구로 하였다. 그리고 2회 처리구는 1회 처리한 과실을 대상으로 예비시험에서 저온저장 중 과실의 에틸렌 발생량이 증가되는 것으로 확인된 저장 2개월 후(자료 미제시) 동일한 방법으로 1회 추가(0.5 + 0.5와 1 + 1µL·L-1) 처리하였다. 과실 저장조건은 온도 0±1°C, 상대습도는 90%로 설정하여 6개월간 저장하였다. 과실의 특성 조사는 1개월 간격으로 수확시를 포함하여 총 7회 실시하였다.
과실 특성 조사
모든 과실은 조사 1일 전 과실을 저장고에서 꺼내어 실온(20°C)에서 품온을 평형시킨 후 처리당 5개의 과실을 1반복으로 하여 3반복 총 15개의 과실을 대상으로 측정하였다. 과실 경도는 직경 11mm plunger를 장착한 과실경도계(Compac-100Ⅱ, Sun Scientific Co., Tokyo, Japan)를 사용하여 과실 적도부의 과피를 제거한 뒤 과실 당 3회 측정한 값을 평균하여 Newton(N)으로 나타내었다. 산 함량은 과즙 5mL를 0.1N NaOH로 적정한 후 사과산으로 환산하였고(DL-15, Mettler Toledo, Greifensee, Switzerland), 가용성 고형물 함량은 디지털당도계(PR-201α, Atago Co., Ltd., Tokyo, Japan)를 이용하여 측정하였다. 과실의 감모율은 수확시 과중을 측정한 후 저장기간 동안 과중의 변화를 측정하여 백분율로 나타냈다. 과피 왁스 발생 정도는 무발생 0, 매우 약한 미끌거림 1, 약간 미끌거림 2, 미끌거림 3, 많이 미끌거림 4, 매우 많이 미끌거림 5로 구분하여 관능적으로 평가하였다(Dadzie et al., 1995). 전분지수는 Cornell Starch Index를 참고하여 관능적으로 평가하였다(Blanpied and Silsby, 1992). 내생 에틸렌 발생량(internal ethylene concentration, IEC)은 주사기를 꽃받침 부위에 삽입하여 과심에서 1mL gas 시료를 채취하였고, FID(flame ionization detector)를 장착한 gas chromatography(GC2010, Shimadzu Co., Kyoto, Japan)를 이용하여 측정하였다. FID 분석조건은 Porapak Q(80/100 1m, Restek, Bellefonte, PA, USA) column을 이용하였고, injector, oven, detector 온도는 각각 100, 90, 200°C로 설정하였고, carrier gas는 He, flow rate는 25mL·min-1로 하였다.
세포벽물질(Alcohol Insoluble Substance, AIS) 추출
세포벽물질 추출은 Rose et al.(1998)이 행한 방법으로 수행하였다. 과피를 제거한 과육 10g에 80% ethanol 100mL를 가한 뒤 항온수조(SH-SAKWB, Samheung21, Korea)에서 40분간 끓인 후 과육을 마쇄하여 여과하였다. 여과 후 남은 잔사는 열처리한 80% ethanol 100mL과 acetone 100mL를 사용하여 차례로 세척하였다. 남은 잔사는 10mM sodium phosphate buffer (pH 7.0)에 넣고 amylase와 protease를 가하여 전분과 단백질을 제거한 후 80% ethanol로 다시 세척하였다. 세척이 끝난 잔사는 30°C의 oven에서 건조시킨 후 이를 세포벽물질(AIS)로 하였다.
Uronic Acid 및 Total Sugar 함량
AIS 10 mg을 이용하여, uronic acid 함량은 carbazole 비색법(Bitter and Muir, 1962)으로 실시하였고, 그 함량은 표준물질인 galacturonic acid를 사용하여 검량선에 의해 산출하였다. Total sugar 함량은 phenol-sulfuric acid 방법(Dubois et al., 1956)으로 정량하였고, 그 함량은 표준물질인 glucose를 사용하여 검량선에 의해 산출하였다.
세포벽분해효소 추출
효소 추출은 Pressey(1983)의 방법으로 행하였다. 과피를 제거한 과육 50g에 10mM sodium phosphate buffer(pH 7.0) 100mL를 가하고, 시료 1g당 0.5mg의 polyvinylpolypyrrolidone를 넣어 10분간 균질화한 다음 1M이 되게 NaCl을 가하여 4시간동안 교반 후 12,000×g에서 60분간 원심분리하여 상등액을 얻었다. 이 상등액을 (NH4)2SO4로 85% 포화·염석하고, 12,000×g에서 60분간 원심분리하여 얻은 침전물을 10mM sodium phosphate buffer(pH 7.0)에 현탁시킨 뒤, 10mM sodium phosphate buffer(pH 7.0) 용액에서 48시간 투석한 다음 22,000 ×g에서 60분간 원심분리한 상등액을 조효소액으로 하였다. 모든 효소의 추출은 4°C에서 행하였다.
세포벽분해효소 활성 측정
β-Galactosidase(β-Gal), α-Galactosidase(α-Gal), β-Glucosidase(β-Glc), α-Mannosidase(α-Man), α-Arabino- sidase(α-Ara) 및 β-Xylosidase(β-Xyl)의 활성들은 각각의 p-nitrophenyl-pyranoside를 기질로 하였을 때 생성되는 p-nitrophenol이 가수분해되는 양을 측정하였다. 즉, 각각의 기질들을 10mM sodium acetate buffer(pH 4.0)에 0.2% 되게 녹인 용액 125µL에 10mM sodium acetate buffer(pH 4.0) 250µL를 가하고 잘 혼합한 후, 효소액 250µL를 가하여 30°C에서 60분간 반응시킨 다음 1M Na2CO3 1mL를 가하여 반응을 정지시키고, UV-VIS spectrophotometer(UV-1800, Shimadzu, Kyoto, Japan) 410nm에서 흡광도를 측정하였다. 각각의 효소 활성도는 30°C에서 1mmol의 p-nitrophenol(min-1·kg-1·FW)이 생성되는 것을 1unit으로 하였다.
통계분석
통계분석은 SPSS 프로그램(IBM SPSS Statistics 20, SPSS Inc., Armonk, NY, USA)을 이용하여 ANOVA 결과 분석 후 과실 품질 항목별로 Duncan 다중검정으로 분석하였다.
결과 및 고찰
수확시 과실 특성
두 품종의 수확시 과실 특성은 Table 1과 같다. ‘썸머프린스’ 과실의 경도는 76.6N, 가용성 고형물 함량은 11.8°Brix, 산 함량은 0.55%, 당산비는 22.6, IEC는 1.1µL·L-1, 왁스는 무발생, 과중은 234.5g으로 품종등록시와 비교하여 다소 작은 과중을 나타냈으며, 전분지수는 2.0으로 과실을 조기에 수확한 것을 확인할 수 있었다. 그리고 ‘썸머킹’ 사과의 경도는 77.2N, 가용성 고형물 함량은 13.4°Brix, 산 함량은 0.40%, 당산비는 33.4, IEC는 25.0µL·L-1, 왁스는 무발생, 전분지수는 5.4였고, 과중은 185.9g으로 ‘썸머프린스’와 같이 품종등록시와 비교하여 다소 작은 과중을 나타냈었다. 과피의 착색 정도는 두 품종 모두 양광면이 부분적 착색이 진행되었으나 낮은 적색도(a*)와 높은 황색도(b*) 값을 나타내어 전형적인 녹색 과실의 착색도를 보였다(Table 1).
Table 1.
Fruit quality attributes in 'Summer Prince' and 'Summer King' apples at harvest
저장기간동안 과실 특성
저장기간에 따른 과실의 경도 변화는 Fig. 1 및 Table 2와 같다. ‘썸머프린스’ 사과의 수확시 경도는 76.6N이었으며, 저장 2개월까지 처리 간 차이를 보이지 않았다. 그러나 무처리구의 경우 저장 3개월부터 경도가 감소하기 시작하여 저장 6개월 후 62.3N으로 감소한 반면, 1-MCP 처리구의 경우 처리 농도 및 횟수와 관계없이 저장 6개월 후 74.2 ‑ 78.6N으로 경도가 현저히 높게 유지되었다(Fig. 1A, p < 0.0001). 그리고 ‘썸머킹’ 과실의 수확시 경도는 77.2N이었고 무처리구의 경우 저장 2개월부터 경도가 급격하게 감소하여 저장 6개월 후 48.6N의 경도를 나타냈으나, 1-MCP 처리구의 경우 처리 농도 및 횟수와 관계없이 저장 6개월 후 61.0 ‑ 63.9N로 무처리구와 비교하여 높은 경도를 유지하였다(Fig. 1B, p < 0.0001). 저장기간동안 ‘썸머프린스’ 사과의 IEC 변화(Fig. 1 and Table 2)는 무처리구의 경우 저장 1개월부터 급격하게 증가하여 저장 4개월 후 469.8µL·L-1로 높은 IEC를 보였으나, 1-MCP 처리구들의 경우 저장 6개월 후에도 21.1 ‑ 31.6µL·L-1로 무처리구와 비교하여 현저히 낮은 IEC를 보였다(Fig. 1C, p < 0.0001). 그리고 ‘썸머킹’ 사과는 무처리구의 경우 저장기간 동안 서서히 증가하여 저장 4개월 후 230.1µL·L-1로 IEC가 증가하였으나, 1-MCP 처리구의 경우 저장 6개월 후에도 처리 농도 및 횟수와 관계없이 36.5 ‑ 51.6µL·L-1로 무처리구와 비교하여 낮은 IEC를 보였다(Fig. 1D, p < 0.0001). 두 품종 모두에서 1-MCP 처리가 과실 경도 유지와 낮은 IEC 유지에 효과적이었으나 1-MCP의 처리 농도와 횟수에 따른 차이는 없었다. Watkins(2007)는 1-MCP가 경쟁적 에틸렌 작용 억제제로서 과실의 에틸렌 작용 억제와 함께 추가적으로 생성되는 에틸렌 발생량을 감소시킴으로써 과실 경도의 감소를 억제하는 데 효과적이라 하였다. Kwon et al.(2017)은 에틸렌 생합성 과정에 Md-ACS1과 Md-ACO1 유전자가 관련되어 있으며, 이 두 유전자의 활성 정도에 따라 에틸렌 발생량에 미치는 영향이 다르다고 하였다. 낮은 에틸렌 발생량과 관련된 대립유전자(favorable alleles)는 ACS1은 2, ACO1은 1이 많을수록 에틸렌 발생량이 낮은 경향을 보인다고 하였는데, ‘썸머프린스’ 사과의 대립유전자형은 ACS1-1/1, ACO1-1/2이고, ‘썸머킹’ 사과는 ACS1-1/2, ACO1-1/2이라고 보고하였다. 따라서 본 연구에서 ‘썸머프린스’ 사과의 IEC가 ‘썸머킹’ 사과와 비교하여 높은 발생량을 나타낸 것으로 판단되었다.
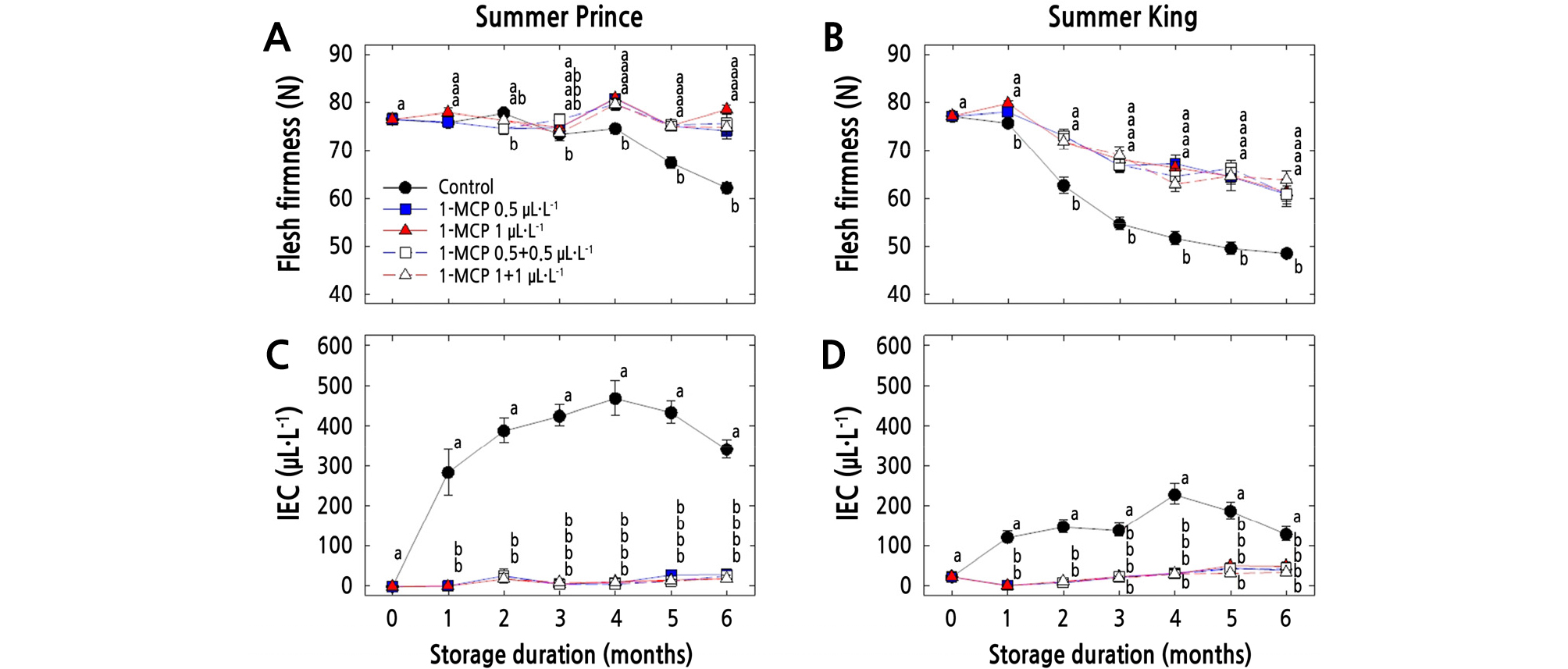
Fig. 1.
Effects of 1-MCP treatments on flesh firmness and internal ethylene concentration (IEC) of cold-stored ‘Summer Prince’ and ‘Summer King’ apples. All values are expressed as mean ± standard error (n=15). Different letters within the column are significantly different at p < 0.05 by Duncan’s multiple range test.
Table 2.
ANOVA result of fruit quality attributes in 1-MCP treated 'Summer Prince' and 'Summer King' apples during cold storage
저장기간 동안 ‘썸머프린스’ 사과의 산 함량(Fig. 2 and Table 2)은 무처리구는 수확 시 0.55%에서 저장 6개월 후 0.16%로 급격히 감소하였으나, 1-MCP 처리구는 0.21 ‑ 0.23%으로 무처리구와 비교하여 높은 산 함량을 유지하였다(Fig. 2C, p < 0.001). 그리고 ‘썸머킹’ 사과의 수확 시 산 함량은 0.40%였으며, 저장 6개월 후 무처리구는 0.17%로 감소하였으나 1-MCP 처리구들은 0.20 ‑ 0.21%로 높은 산 함량을 유지하였다(Fig. 2D, p < 0.01). 그리고 가용성 고형물 함량 변화를 보면(Fig. 1, Table 2), ‘썸머프린스’ 사과의 경우 수확시와 비교하여 저장 2개월까지 가용성 고형물의 함량이 다소 증가하는 경향을 나타냈으나 1-MCP 처리에 따른 뚜렷한 차이는 없었고(Fig. 2A), ‘썸머킹’ 사과 역시 유사한 경향을 보였다(Fig. 2B). DeEll et al.(2016)은 ‘McIntosh’와 ‘Empire’ 사과에 1-MCP를 수확 직후 처리하거나 저장 4개월 후 추가 처리하였을 때 저장 9개월 후 가용성 고형물 함량의 변화는 없다고 하였다. 저장기간별 당산비의 변화를 보면(Fig. 2 and Table 2), ‘썸머프린스’ 사과는 수확 시 22.6에서 무처리구는 저장기간이 경과함에 따라 산 함량이 감소하여 저장 6개월 후 77.6을 보였고, 1-MCP 처리구들의 경우 산 함량 감소가 억제되어 54.4 ‑ 59.5의 당산비를 나타내었다(Fig. 2E, p < 0.01). 그리고 ‘썸머킹’ 사과 역시 수확 시 33.4에서 저장 6개월 후 무처리구의 경우 79.9의 당산비를 나타냈으나, 1-MCP 처리구는 64.6 ‑ 69.3의 당산비를 보여(Fig. 2F, p < 0.01) 과실의 신선도가 유지된 것을 확인할 수 있었다. 사과 과실은 수확 후에도 호흡, 증산 및 에틸렌 생성과 같은 일련의 대사활동이 계속되며 이때 유기산이 일부 호흡기질로 이용되어 산 함량이 감소하게 되는데 1-MCP가 호흡을 억제하여 산 함량의 감소를 억제시킨다고 하였다(Rupasinghe et al., 2000; Toivonen and Lu, 2005). 대표적인 국내 재배품종인 ‘후지’, ‘홍로’, 그리고 ‘감홍’ 사과 역시 수확 후 1-MCP를 처리하였을 때 저장기간 동안 과실의 산 함량과 경도가 높게 유지된다고 보고되었으며(Lim et al., 2007, 2009; Yoo et al., 2013, 2015), 본 결과에서도 이와 동일한 경향을 보였다.
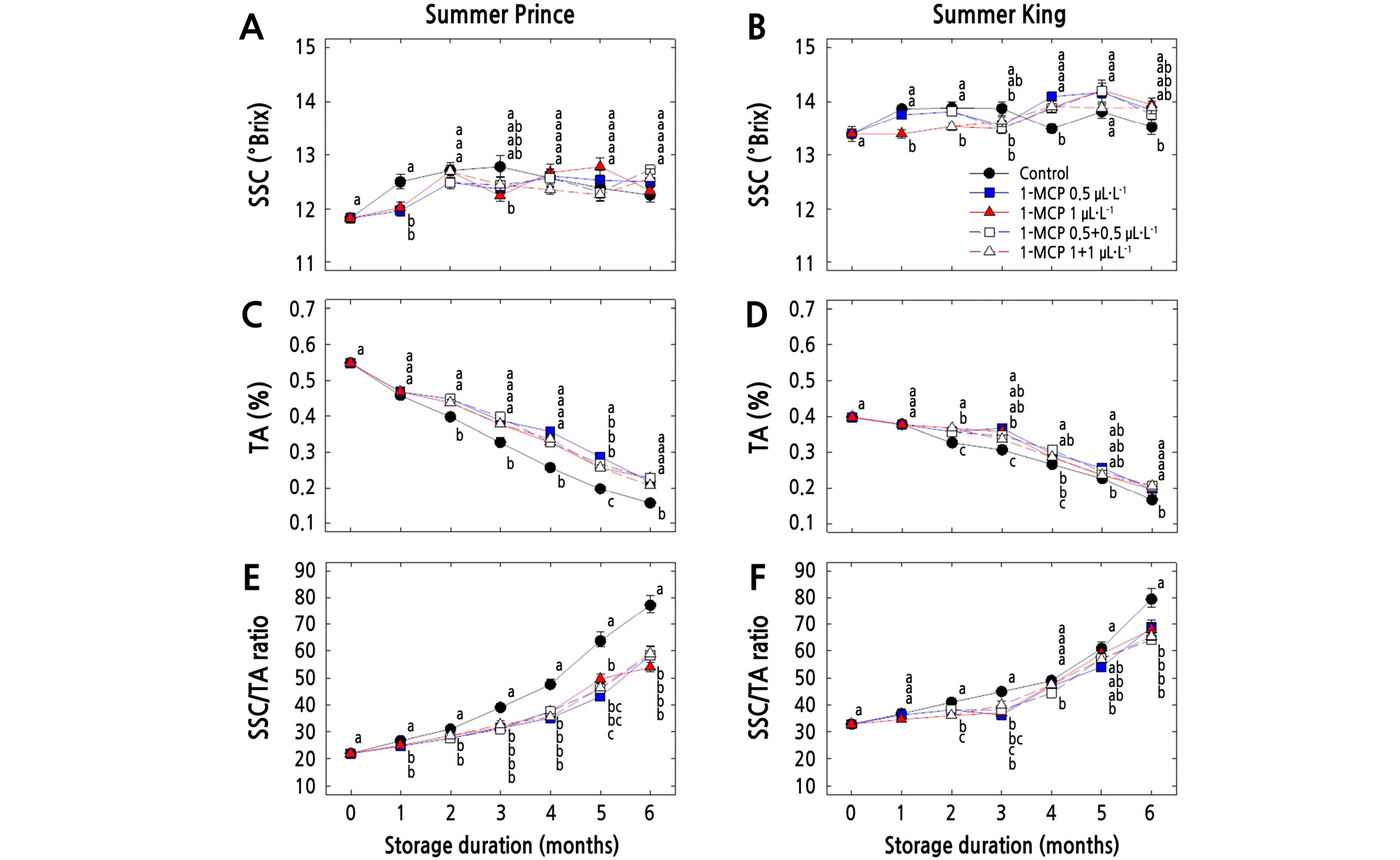
Fig. 2.
Effects of 1-MCP treatments on soluble solids content (SSC), titratable acidity (TA), and SSC/TA ratio of cold-stored ‘Summer Prince’ and ‘Summer King’ apples. All values are expressed as mean ± standard error (n=15). Different letters within the column are significantly different at p < 0.05 by Duncan’s multiple range test.
저장기간에 따른 감모율의 변화를 보면(Fig. 3 and Table 2), ‘썸머프린스’ 사과는 저장기간이 경과함에 따라 서서히 증가하여 저장 6개월 후 무처리구는 3.0%의 감모율을 나타냈으나, 1-MCP 처리구들은 2.5 ‑ 2.7%로 무처리구와 비교하여 낮은 감모율을 보였다(Fig. 3A, p < 0.01). ‘썸머킹’ 사과는 저장 6개월 후 1-MCP 처리구의 감모율은 1.9 ‑ 2.1%를, 무처리구는 2.2%로 큰 차이를 보이지 않았다(Fig. 3B). 저장기간 동안 전분지수의 변화를 보면(Fig. 3 and Table 2), ‘썸머프린스’와 ‘썸머킹’ 사과는 수확 시 각각 2.0과 5.4를 나타냈었고 이후 저장기간이 경과함에 따라 점차 증가하여 각각 저장 5개월과 4개월후 전분지수 8.0으로 전분분해가 완료되었으며 처리 간 차이를 보이지 않았다(Fig. 3C and 3D). 그리고 두 품종 모두 저장기간 동안 과피 왁스는 발생되지 않았다(Fig. 3E and 3F). 그리고 저장기간 동안 두 품종 모두에서 생리장해는 관찰되지 않았다(자료 미제시). 과실의 성숙 정도를 판단하는데 이용되는 전분함량의 변화는 에틸렌 발생과 호흡률의 증가 같은 환경적, 생리적 변화와 높은 관련이 있으며(Brookfield et al., 1997; Magein and Leurguin, 2000), 미숙한 상태에서 수확한 ‘Tsugaru’와 ‘Fuji’ 사과의 경우 1-MCP 처리가 에틸렌 발생량의 증가는 억제하지만 전분함량의 감소에 미치는 영향은 적다고 보고하였다(Rupasinghe et al., 2000; Pre-Aymard et al., 2003; Thammawong and Arakawa, 2007). 그리고 사과 품종에 따라 저장기간 동안 발생되는 왁스의 구성성분 및 발생 정도는 차이를 보이지만(Veraverbeke et al., 2001; Curry, 2008), ‘썸머프린스’와 ‘썸머킹’ 사과의 경우 과피의 왁스 발생 정도가 매우 낮은 품종이라 판단되었다.
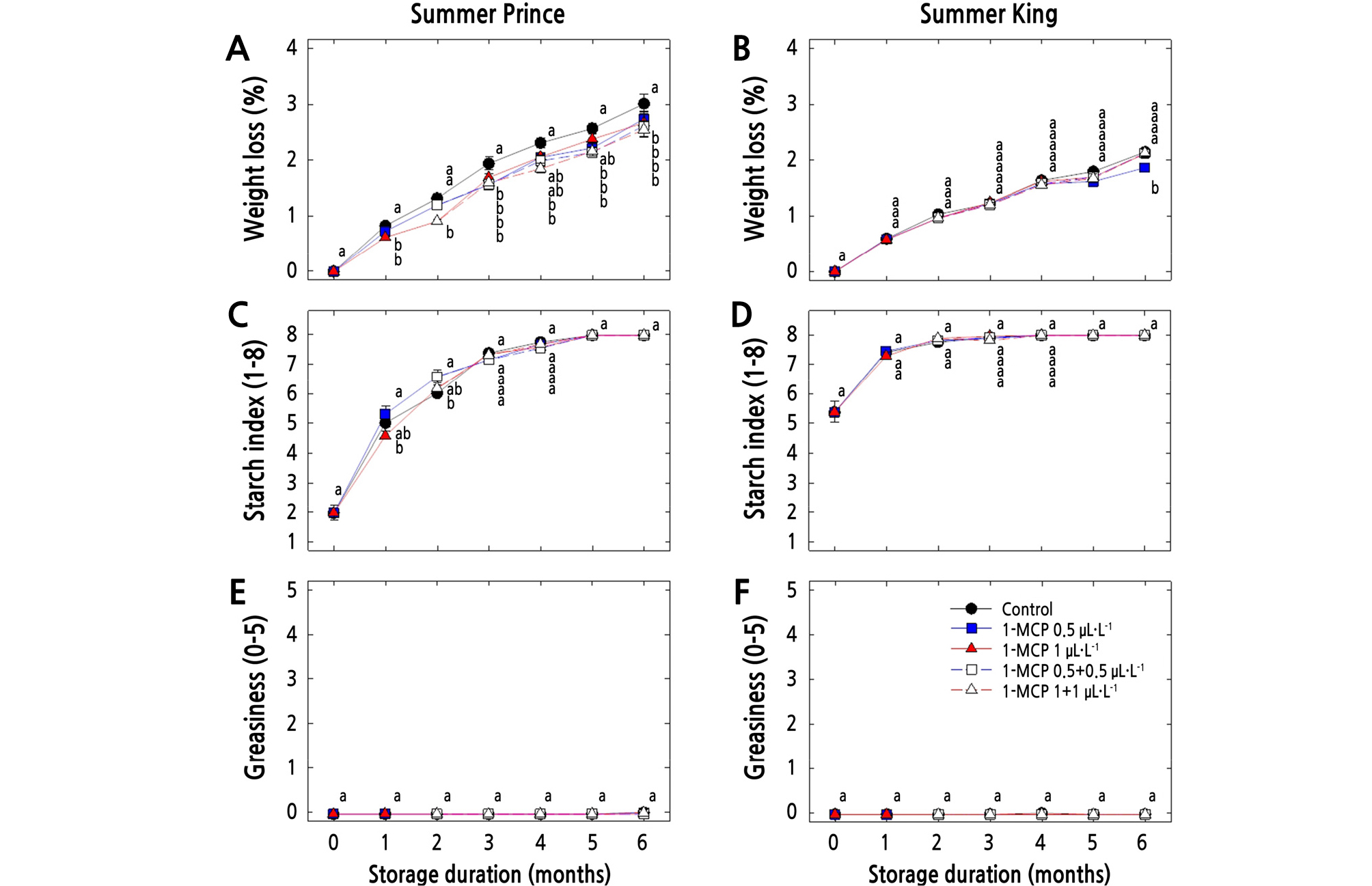
Fig. 3.
Effects of 1-MCP treatments on weight loss, starch index, and greasiness of cold-stored ‘Summer Prince’ and ‘Summer King’ apples. All values are expressed as mean ± standard error (n=15). Different letters within the column are significantly different at p < 0.05 by Duncan’s multiple range test. The level of starch index was assessed subjectively at eight levels and quantified as 1 (least mature) to 8 (completely mature). The level of greasiness was assessed subjectively at six levels and quantified numerically as 0 (none), 1 (slight), 2 (light moderate), 3 (moderate), 4 (light severe), or 5 (severe).
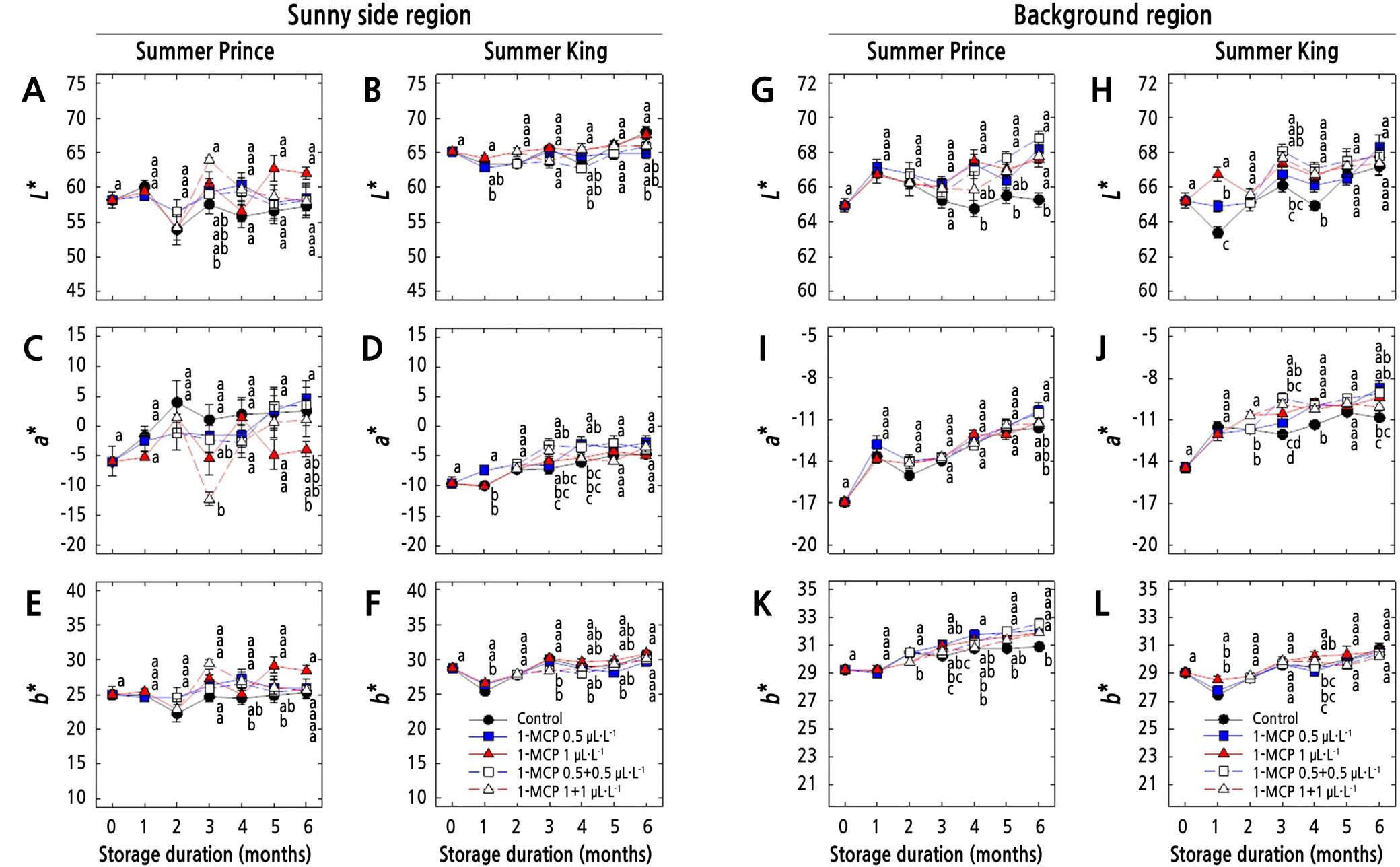
저장기간 동안 착색이 진행된 양광면(Sunny side)과 바탕색(Background)의 착색 변화를 보면 다음과 같다(Fig. 4 and Table 2). ‘썸머프린스’ 사과의 바탕색 명도(L*)는 무처리구의 경우 수확 시 65.0에서 저장 6개월 후 65.3으로 변화를 보이지 않았으나 1-MCP 처리구들의 경우 67.6 ‑ 68.8로 무처리구와 비교하여 높은 명도를 나타냈다(Fig. 4G, p < 0.01). 바탕색의 황색도(b*) 역시 저장기간이 경과함에 따라 1-MCP 처리구들의 경우 점차 증가하는 경향을 나타냈으나 무처리구의 경우 다소 낮은 황색도를 나타내었고(Fig. 4K), 바탕색 적색도(a*)는 처리 간 차이를 보이지 않았다(Fig. 4I). 양광면의 착색 변화는 저장기간 동안 1-MCP 처리에 따른 뚜렷한 차이는 확인되지 않았다(Fig. 4A, 4C and 4E). ‘썸머킹’ 사과의 경우 저장기간 동안 양광면과 바탕색의 명도, 적색도, 그리고 황색도 모두 점차 증가하는 경향을 나타냈으나 1-MCP 처리에 따른 차이는 확인되지 않았다(Fig. 4B, 4D, 4F, 4H, 4J and 4L). Blankenship and Dole(2003)은 사과에 1-MCP를 처리하였을 때 저장기간 동안 착색 변화를 지연시킨다고 하였으나, Mattheis et al.(2017)은 ‘Honeycrisp’ 사과에 1-MCP를 처리하였을 때 저장기간동안 무처리구와 비교하여 착색 변화에 미치는 영향이 없다고 하였다. 이상의 결과 과실의 품종에 따라 1-MCP 처리에 따른 착색 변화 정도는 차이를 보이며, ‘썸머킹’ 품종은 1-MCP 처리에 따른 착색 변화가 적은 품종이라고 판단되었다.
Total Sugar(TS)와 Uronic Acid(UA)의 함량
일반적으로 알려진 과실의 연화 현상은 세포벽 구성성분 및 구조의 변화에 따라 발생하게 된다. 따라서 저장기간 동안 ‘썸머프린스’와 ‘썸머킹’ 사과의 세포벽 중층 구성물질인 TS와 UA 함량의 변화를 보면 Fig. 5 및 Table 2와 같다. ‘썸머프린스’ 사과의 TS 함량은 무처리구의 경우 저장기간이 경과함에 따라 서서히 감소하여 저장 6개월 후 71.7µg·mg-1 AIS로 감소하였으나, 1-MCP 처리구들의 경우 85.2 ‑ 86.7µg·mg-1 AIS로 무처리구와 비교하여 높은 TS 함량을 유지하였다(Fig. 5A, p < 0.0001). 그리고 UA 함량 역시 무처리구의 경우 저장 6개월 후 66.6µg·mg-1 AIS로 감소하였으나, 1-MCP 처리구들은 99.1 ‑ 102.7µg·mg-1 AIS로 높은 UA 함량을 유지하였다(Fig. 5C, p < 0.0001). ‘썸머킹’ 사과의 UA 함량은 무처리구의 경우 저장 6개월 후 71.5µg·mg-1 AIS로 감소하였으나, 1-MCP 처리구들의 경우 81.4 ‑ 91.3µg·mg-1 AIS로 무처리구와 비교하여 높은 UA 함량을 유지하였고(Fig. 5D, p < 0.01), TS 함량은 저장기간 동안 처리에 따른 뚜렷한 차이가 확인되지 않았다(Fig. 5B). 세포의 일차세포벽 사이에 존재하는 세포벽 중층은 펙틴질과 함께 galacturonic acid, rhamnose, arabinose, galactose와 같은 sugar group으로 이루어져 있으며, 1-MCP를 처리하였을 때 펙틴질과 sugar group의 분해 및 유리를 지연시켜 UA와 TS 함량을 높게 유지시키고 과실의 연화를 억제한다고 하였다(Gross and Wallner, 1979; Gross, 1983; Huber, 1983; Yoo et al., 2018). 따라서 1-MCP 처리가 두 품종의 저장 중 세포벽 중층을 구성하고 하는 TS와 UA의 함량 변화를 억제하여 과실의 저장성이 유지된 것으로 판단되었다.
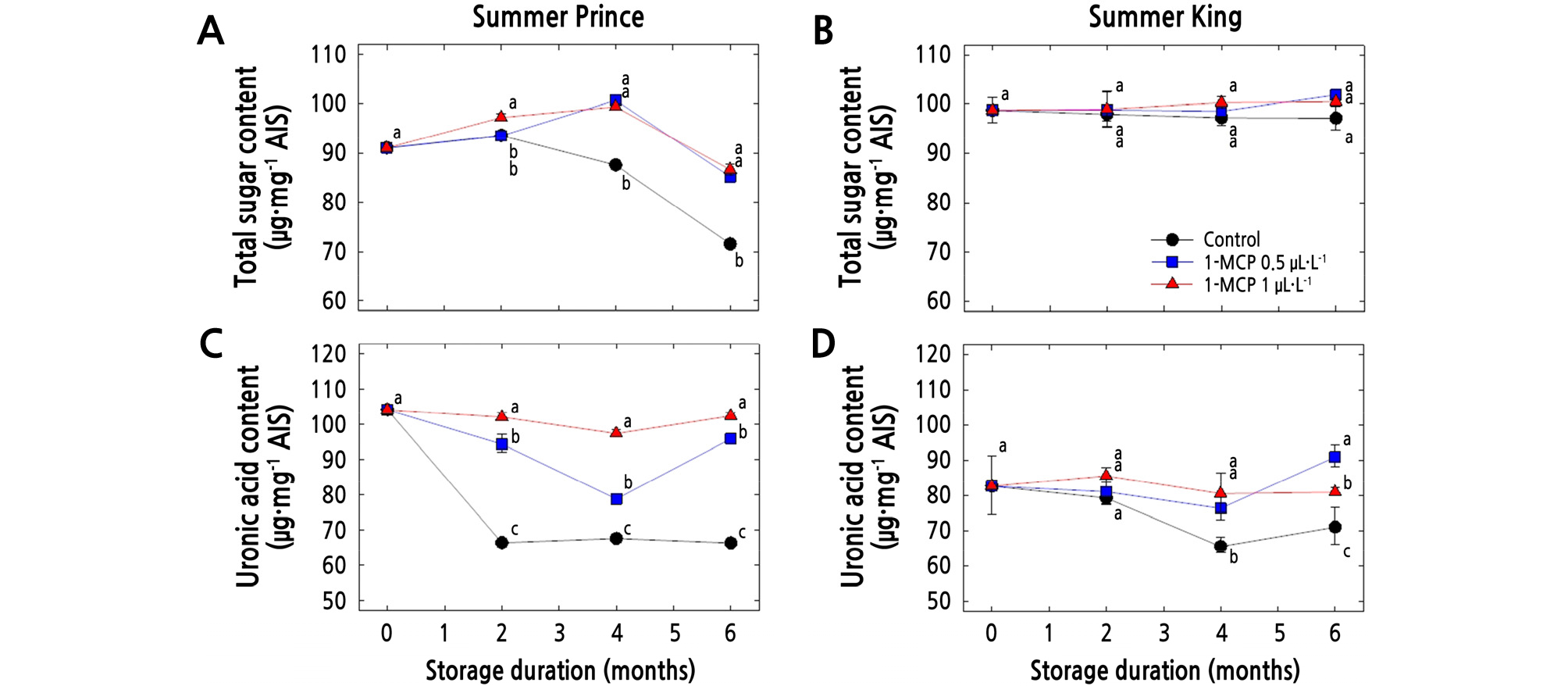
Fig. 5.
Effects of 1-MCP treatments on total sugar content and uronic acid content of cold-stored ‘Summer Prince’ and ‘Summer King’ apples. All values are expressed as mean ± standard error (n=3). Different letters within the column are significantly different at p < 0.05 by Duncan’s multiple range test.
세포벽분해효소 활성 변화
저장기간에 따른 세포벽분해효소의 활성 변화는 Fig. 6 및 Table 2와 같다. ‘썸머프린스’ 사과의 β-Gal는 저장기간이 경과함에 따라 점차 증가하여 무처리의 경우 저장 4개월 후 76.5units kg-1으로 급격히 증가하였으나 1-MCP 처리구들의 경우 무처리구와 비교하여 낮은 효소 활성을 보였다(Fig. 6A). 그리고 α-Gal, β-Glc, α-Man, 및 α-Ara 역시 무처리구의 경우 저장기간이 경과함에 따라 점차 증가하여 저장 4개월 후 높은 효소 활성을 나타내었으나, 1-MCP를 처리하였을 때 낮은 효소 활성을 보였다(Fig. 6C, 6E, 6G, 6I and 6K). ‘썸머킹’ 사과는 무처리구의 경우 β-Gal, β-Glc, β-Xyl 및 α-Ara의 활성이 저장 2개월까지 다소 증가한 뒤 감소하였으나, 1-MCP를 처리하였을 때 무처리구와 비교하여 낮은 효소 활성을 보였다(Fig. 6B, 6D, 6F, 6H, 6J and 6L). 세포벽의 붕괴에는 펙틴을 분해하는 세포벽분해효소들이 관여하고 있으며(Knee, 1978), 에틸렌 발생량이 증가하였을 때 이들 효소의 활성을 증가시켜 과실의 연화를 초래한다고 하였다(Yamaki and Matsuda, 1977; Bartley and Knee, 1982; Yoo et al., 2018). 특히, β-Gal의 활성 증가는 펙틴질의 측쇄인 galactan과 arabinogalactan을 galactose와 arabinose로 유리시켜 과실 연화의 주요인으로 보고된 바 있다(Bartley, 1974). 그리고 Byun et al.(1993)은 사과 품종의 유전적 특성의 차이로 인하여 품종별 효소 활성의 차이를 보인다고 하여 본 연구에서도 상이한 효소 활성을 나타낸 것으로 판단된다.
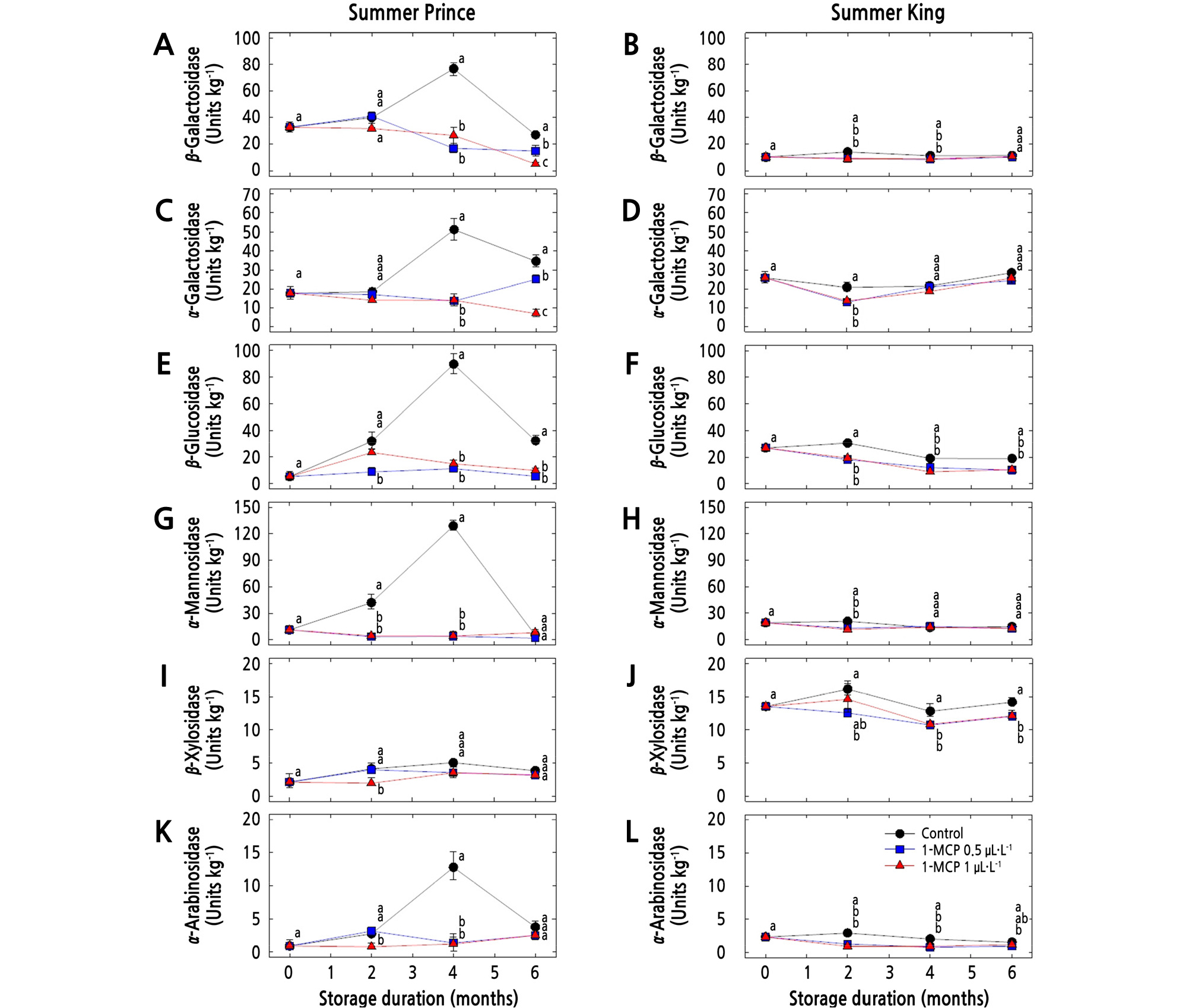
Fig. 6.
Effects of 1-MCP treatments on cell wall hydrolases activities of cold-stored ‘Summer Prince’ and ‘Summer King’ apples. All values are expressed as mean ± standard error (n=3). Different letters within the column are significantly different at p < 0.05 by Duncan’s multiple range test. *One unit of enzyme was defined as the amount of activity released from 1 mmol of p-nitrophenol per kg per min on a fresh weight basis.
상관관계 분석
수확 후 1-MCP 처리가 ‘썸머프린스’와 ‘썸머킹’ 사과의 저온저장 중 과실 품질과 세포벽물질 변화에 미치는 상관관계는 Fig. 7과 같다. ‘썸머프린스’ 사과의 세포벽분해효소들 간 상관관계를 살펴보면 무처리구의 경우 높은 정의 상관관계(r = 0.652* ‑ 0.987**)를 보였으나, 1-MCP 처리구들의 경우 r = ‑ 0.185 ‑ 0.909**로 상관관계가 낮았다. 그리고, IEC는 세포벽분해효소들과 무처리구의 경우 정의 상관관계(r = 0.376 ‑ 0.632*)를 보였으나, 1-MCP 처리구들의 경우 r = ‑ 0.888** ‑ 0.602*로 상관관계가 감소였으며 경우에 따라 높은 부의 상관관계를 보였다. 저장기간 동안 과실의 품질을 평가하는 대표적인 요인인 경도와 산 함량 역시 상이한 상관관계를 보이고 있다. 무처리구의 경우 r=0.649**로 높은 정의 상관관계를 보였으나, 1-MCP 처리구들의 경우 각각 r = ‑ 0.130 ‑ 0.186로 상관관계가 감소하였다. ‘썸머킹’ 사과 역시 위와 동일한 결과를 나타냈으며, 세포벽분해효소들 간의 상관관계는 ‘썸머프린스’ 사과와 비교하여 다소 감소하였다. 이는 수확 후 처리되는 1-MCP가 에틸렌 생성 감소, 경도와 산 함량 유지 등 과실의 품질을 유지시키고 세포벽분해효소의 활성을 억제시킴으로써 처리 간 상이한 상관관계를 나타내는 것으로 판단된다(DeEll et al., 2007; Watkins, 2007).
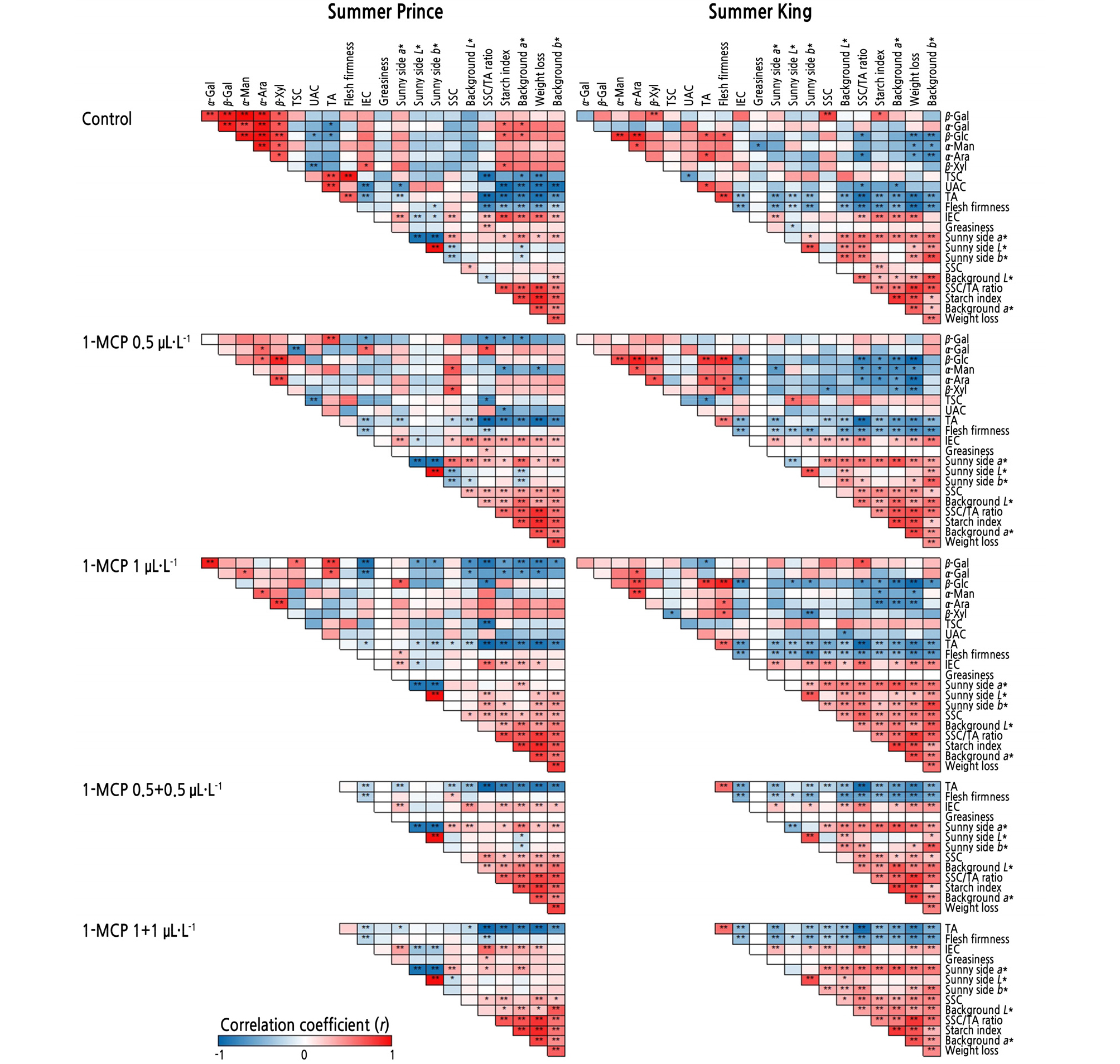
Fig. 7.
Correlation coefficients (r) between fruit quality attributes and enzymatic activities of cell wall hydrolases of cold-stored ‘Summer Prince’ and ‘Summer King’ apples treated with different application concentration of 1-MCP treatments. The red and blue colors indicate positive and negative correlations between fruit quality attributes and enzymatic activities of cell wall hydrolases, respectively. β -Gal: β -Galactosidase, α -Gal: α -Galactosidase, β -Glc: β -Glucosidase, α -Man: α -Mannosidase, α -Ara: α -Arabinosidase, β -Xyl: β -Xylosidase, TSC: total sugar content, UAC: uronic acid content, TA: titratable acidity, SSC: soluble solids content, IEC: internal ethylene concentration. Asterisks (* or **) indicate statistically significant correlation at p < 0.05 or 0.01, respectively.
따라서 이상의 결과를 종합해 보면, 국내 육성 조생종 사과인 ‘썸머프린스’와 ‘썸머킹’에 대한 1-MCP 처리는 과실 품질과 세포벽 대사물질 변화 억제에 효과적이었다. 그리고 1-MCP 처리 농도 및 횟수에 따른 차이는 없어 0.5µL·L-1 1-MCP의 1회 처리가 유용한 방안이라고 판단되었다.