서 언
재료 및 방법
실험식물
유전자원 형질 조사, 수확 및 과실 특성 조사
과실 품질 조사
비타민 C 함량 측정
유기산 함량 측정
통계처리
결과 및 고찰
키위프루트 유전자원의 특성
다변량 분석
서 언
키위프루트(Kiwifrut, Actinidia spp.)는 다래나무과(Actinidiaceae) 다래나무속(Actinidia)에 속하는 덩굴성 낙엽과수로 뉴질랜드, 중국, 이탈리아, 칠레 등을 중심으로 상업적 재배가 이뤄지고 있다. 다래나무속에는 60여 개의 다양한 종이 분포하고 있는데, 각각의 종에 따라 변이가 많아 잠재적 유용성을 가지고 있다(Ferguson, 1999b). 과중, 과형, 과피색, 과피털, 식미, 과육색, 질감, 향기, 기능성 물질과 같은 과일 특성을 비롯해 성숙기, 저장기간 등 다양성을 가지고 있다(Huang et al., 2004; Ferguson, 2007; Ferguson and Huang, 2007). 이 외에도 수세, 발아기, 개화기, 병해충 저항성, 수량성 등에서 많은 차이를 나타낸다. 같은 종 내에서도 상당한 다양성을 보이며 형태적인 특성에서 차이를 보이지 않더라도, 생리적 반응에서 큰 차이를 나타내기도 한다(Ferguson, 2007). 이러한 유전적 다양성을 기반으로 각 나라의 키위프루트 육종 프로그램은 다양한 모양과 크기의 과일, 녹색이 아닌 황색, 붉은 색과 같은 다른 색의 과육, 과피에 털이 없는 과일 등 다양한 품종을 개발하였다(Muggleston et al., 1998; Ferguson, 1999a; Huang et al., 2002; Wang et al., 2003; Zhong et al., 2007; Sotiropoulos, 2009).
최근 들어 지구온난화의 영향으로 기후가 점점 변하고 있고 궤양병과 같이 방제가 어려운 병과 돌발 해충으로 인한 피해가 늘어나고 있어 새로운 품종의 요구가 증가하고 있다. 또한, 산업의 발전과 더불어 소득이 증가하고 다양한 과일을 접하면서 소비자의 기호가 다양해져 새로운 품종에 대한 수요가 증가하고 있다. 이러한 변화에 대응하기 위해 다양한 품종 개발을 위한 육종 프로그램이 필요하며 유전자원의 특성 평가와 유용자원 선발이 실시되어야 한다. 유전적 다양성을 기반으로 꾸준히 선발을 한다면 환경 변화와 돌발 병해충에 대응이 가능하고 급속한 소비 트렌드 변화에도 대응할 수 있다(Simmonds, 1962; Ferguson, 2007).
중국과 뉴질랜드를 중심으로 형태적 특성을 이용한 유전자원 평가가 진행되었고, 기초 생리적 특성을 이용한 유전자원 연구도 수행되었다(Thorp et al., 1990; Huang et al., 2004). 일본에서는 다래나무속 중 A. arguta와 A. rufa 유전자원에 대한 과실 특성 및 후숙 특성 평가와 더불어 육종 소재로서의 활용 가능성을 평가하였다(Kim et al., 2009b; Kim et al., 2009c; Kim et al, 2012). 또한, 과육 내 적색을 가진 유전자원과 A. arguta 유용자원을 선발하기 위한 특성 평가를 수행하였고 A.arguta 유전자원의 건강증진 성분에 대한 연구가 수행되었다(Latocha and Krupa, 2007; Wang et al., 2012; Baranowska-Wójcik and Szwajgier, 2019). 또한 궤양병 저항성과 과일 특성의 상관관계를 밝혔으며(Cheng, 2014), 배수성과 과일 특성의 상관관계에 대한 연구도 수행되었다(Li et al., 2010). 국내에서는 다래나무속 유전자원에 대해 GBS(genotyping-by-sequencing) 기술을 이용하여 유전적 다양성을 평가하고 핵심집단을 작성하였다(Oh et al., 2019).
우리나라는 140여점의 다래나무속 유전자원을 보존하고 있으며 이 유전자원들을 이용해 황색 과육 품종인 ‘Jecy Gold’, 껍질째 먹을 수 있는 ‘Skinny Green’, 과육 내 적색을 띄는 ‘Redvita’ 등 다양한 품종이 육성되어 보급되었다(Kim et al., 2007; Kwack et al., 2008; Kim et al., 2009a; Kwack et al., 2010; Kim et al., 2012; Kwack et al., 2017a, 2017b; Kim et al., 2018). 하지만 이에 비해 유전자원 연구는 미흡하며 기초자료도 부족한 실정이다.
따라서 본 연구는 국내 보존 중인 다래나무속 자원 중 주요 재배종인 A. deliciosa 종과 A. chinensis 종의 특성 조사와 다변량 분석으로 계통 선발에 유용한 형질을 파악하고 유용 형질별로 자원을 분류하여 육종 프로그램의 기초자료로 활용하고자 수행되었다.
재료 및 방법
실험식물
국립원예특작과학원 남해출장소에서 보존 중인 키위프루트 유전자원 28점을 실험재료로 사용하였고, 유전자원 목록은 Table 1과 같다. 보존 포장은 사각 밀폐식 방풍망(청색, 4mm)으로 덮여 있으며 재식거리는 주간 4m, 열간 4m였다. 키위프루트 유전자원은 평덕형 수형으로 관리하였다.
Table 1.
Twenty-eight kiwifruit accessions included in this study
유전자원 형질 조사, 수확 및 과실 특성 조사
발아기 조사는 3월 하순에서 4월 상순에 실시하였고, 발아의 판단 기준은 신초가 1cm 이상 자란 것을 기준으로 전체 눈에서 50% 이상이 발아한 때를 발아기로 하였다. 꽃차례는 꽃봉오리가 생장하여 개화 전인 4월 중순에 수관 전체에서 우점하는 꽃차례로 하였다. 만개기는 개화가 시작되는 5월부터 전체 꽃봉오리 중 60%가 개화된 시점을 조사하였다.
과실 수확은 가용성 고형물 함량이 7.5 ‑ 8.5°Brix에 도달했을 때 실시하였고, 수확과 동시에 과경장을 조사하였다. 수확된 과실은 저온저장고에 온도 1°C, 상대습도 90% 조건에 저장하였다. 과실 특성은 저장 1개월 후, 15°C에서 에틸렌 발생제(Fresh Ripe, Topfresh, Seoul, Korea)를 사용하여 후숙시킨 후 경도가 2.5kg·cm-2 이하일 때 조사하였다.
조사항목은 과중, 종경, 횡경, 경도 및 가용성 고형물 함량, 산 함량, 비타민 C, 유기산 함량이었으며, 이들의 분석을 위하여 유전자원 당 10반복으로 실시하였다. 비타민 C와 유기산 함량은 2017년에 조사하였고, 이외의 모든 형질은 2016년부터 2017년까지 2년간 조사하였다.
과실 품질 조사
가용성 고형물 함량은 과실을 횡으로 3등분한 후, 중앙 부분을 4등분하여 과즙을 낸 후 굴절당도계(PR-32α, ATAGO, Tokyo, Japan)를 이용하여 측정하였다. 경도는 과피를 2mm 두께로 잘라낸 후 과실경도계(FHM-5, Fujiwara Scientific Co., Tokyo, Japan)를 사용하여 12mm 원형 probe로 측정하였다. 산 함량 측정은 증류수 40mL에 과즙 10mL을 가한 용액을 자동적정기(TitroLineⓇ 5000, SI Analytics, Mainz, Germany)를 이용하여 0.1N NaOH 용액으로 pH 8.2가 될 때까지 적정한 후, 구연산 함량으로 환산하였다.
비타민 C 함량 측정
비타민 C 분석은 액체 크로마토그래피(YL9100, Young Lin Instrument Co., Anyang, Korea)를 이용하여 분석하였다. 후숙된 과일의 과육 2g을 5% meta-phosphoric acid 10mL에 마쇄한 후, 4°C, 7,000×g에서 5분간 원심분리하여 상징액을 채취하였다. 0.45µm 멤브레인 필터(Syringe filter, Macherey-Nagel, Düren, Germany)에 여과된 상징액을 분석에 이용하였다. Column은 ZORBAX Eclipse XDB-C18(4.6 × 150mm, 5µm particle size) column(Agilent Technologies, Santa Clara, CA, USA)을 사용하였고, 이동상은 HCl을 이용해 pH 3.0으로 적정된 0.05 M KH2PO4를 사용하였다. 주입량은 20µL로 하였고 유속 1.0mL·min-1 조건에서 UV-vis Detector를 이용하여 254nm에서 측정하였다. 표준물질은 L-ascorbic acid (Sigma-Aldrich, St. Louis, MO, USA)를 사용하였다.
유기산 함량 측정
키위프루트는 과육 부위에 따라 3가지 유기산 분포의 차이가 있다. 내과피에 구연산 함량이 가장 높고 외과피에는 퀸산의 함량이 높다. 과심은 총 유기산 함량이 가장 적지만 대부분 구연산이므로 과일을 균등하게 채취하는 것이 중요하다(Marsh et al., 2004). 유기산 측정을 위하여 후숙된 과일의 과육 2g을 증류수 10mL에 마쇄한 후, 4°C, 7,000×g에서 5분간 원심분리하여 상징액을 채취하였다. 0.45µm 멤브레인 필터(Syringe filter, Macherey-Nagel, Düren, Germany)에 여과된 상징액을 액체 크로마토그래피(YL9100, Young Lin Instrument Co., Anyang, Korea)로 분석하였다.
분석 조건은 Weikle(2012)과 Nishiyama et al.(2008)의 방법을 변형시켜 적용하였다. Column은 ZORBAX Eclipse XDB-C18(4.6 × 150mm, 5µm particle size) column(Agilent Technologies, Santa Clara, CA, USA)을 사용하였고, 이동상은 HCl을 이용해 pH 2.8로 적정된 0.05 M KH2PO4를 사용하였다. 주입량은 시료 20µL로 1.0mL·min-1 유속에서 UV-Vis Detector를 이용하여 214nm에서 측정하였다. 표준물질은 citric acid, (‑) quinic acid, 그리고 D-malic acid(Sigma-Aldrich, St. Louis, MO, USA)를 사용하였다.
통계처리
변수의 통계처리와 다변량 분석은 SAS Enterprise Guide 4.3(SAS Institute Inc., Cary, NC, USA)을 사용하였다.
결과 및 고찰
키위프루트 유전자원의 특성
본 실험에 사용된 키위프루트 유전자원 28점에 대한 형태적 형질은 Table 2와 같다. 대부분의 자원이 3월 하순에 발아했으나, ‘Hayward’와 ‘Gracies’, ‘Jecy Green’의 발아기는 4월 상순으로 다른 자원에 비해 다소 늦은 경향을 보였다. 최근 들어 온난화의 영향으로 겨울철이 따뜻해지고 있다. 이러한 현상이 계속된다면 저온요구도가 부족해질 것이고 발아기가 빨라져 저온 피해 발생률이 높아질 것이다.
Table 2.
Morphological characteristics of kiwifruit accessions
과수 재배에서 저온요구도는 효과적이고 균일한 발아와 개화를 위한 선행 조건으로 휴면 충족을 위해 매우 중요하다(Sunley et al., 2006). 키위프루트는 휴면에 들어간 후, 발아와 개화를 위해 최소한의 저온 시간이 필요하다(Wall et al., 2008). Caldwell(1989)은 ‘Hayward’는 영양눈의 생장을 위해서는 950시간 이상의 저온요구도가 필요하다고 했다. Kwack et al.(2017)의 연구에서 국내 키위프루트의 재배조건(노지, PE 필름 피복, 청색 또는 백색 파풍망 피복)에서 3가지 모델(Sunley et al., 2006)을 적용하여 계산한 결과, 1,400시간 이상 충족에는 문제가 없다고 보고했다. 하지만, 제주도의 경우 겨울철 온도가 따뜻하고 PE 필름 피복재배가 대부분이므로 저온요구도 충족 여부와 발아, 개화에 미치는 영향에 대한 추가 연구가 필요하다고 언급했다.
위의 연구 결과를 비추어 보았을 때, 따뜻한 겨울철이 계속된다면 키위프루트의 발아와 개화에 필요한 저온요구도가 부족해질 것으로 생각되며, 저온요구도가 낮은 품종을 육성하기 위해 유전자원별 저온요구도를 측정하고 분류하여 유용한 유전자원의 선발이 먼저 수행되어야 할 것으로 판단된다.
따뜻한 겨울철과 재배지역의 북상(전라북도, 경기도 등)으로 봄철 서리 피해 방지는 안정적인 재배에 있어 중요한 요소로 작용할 것이다. 따라서, 발아기가 늦은 ‘Hayward’, ‘Jecy Green’과 같은 유전자원을 활용하여 발아기 서리 피해를 최소화할 수 있는 품종 육성이 필요할 것으로 판단된다.
A. deliciosa 유전자원의 만개기는 5월 15 ‑ 22일로 모든 유전자원이 5월 15일 이전에 만개한 A. chinensis 유전자원에 비해 늦은 경향을 보였다. 꽃차례는 28자원 중 21자원이 홑꽃차례였고, 기산꽃차례가 ‘SKK33’, ‘Sensation apple’, ‘SKK5’, ‘Halla Gold’, ‘Goldone’, ‘Sweet Gold’로 6자원이었으며 다산꽃차례가 ‘Haeguem’ 1자원으로 조사되었다. 키위프루트는 생리적인 낙과가 없어 과일의 품질관리를 위해 적뢰가 필요한데 기산꽃차례 또는 다산꽃차례를 가진 품종은 측화 발생이 많아 적뢰 작업에 많은 노동력이 투입된다. 본 연구에서 조사된 홑꽃차례 자원은 적뢰 노동력을 절감시키는 생력형 품종 육성에 좋은 교배 집단으로 사용될 수 있을 것으로 판단된다. 키위프루트의 꽃차례는 수세, 기후의 영향에 따라 측화 발생이 달라져 수관 전체가 동일한 꽃차례를 가지지 않는다. 생력형 품종 육성을 위한 유전자원 기초자료에 사용되기 위해선 꽃차례라는 질적 변수보다 결과지당 측화 발생량이라는 양적 변수를 사용해야 할 것으로 판단되고, 이는 다변량 분석에도 유용하게 사용될 것이다.
수확기는 10월 20일인 ‘Hongyang’부터 11월 15일인 ‘Hayward’까지 약 25일간 분포되어 있다. A. chinensis 종의 유전자원은 대부분 11윌 이전에 수확이 가능하며, A. deliciosa 종의 유전자원은 ‘Garmrok’을 제외하면 11월 이후에 수확이 가능했다. 키위프루트에서 수확기 기상은 과일의 생산, 그리고 수확 후 관리에 있어 아주 중요한 요소다. 주산지에서 수확기가 11월 중순으로 늦은 경우 수확기의 불규칙한 기온변화로 인한 저온과 서리 피해에 대응하기 어렵다. 서리 피해 예방을 위해 조기 수확할 경우 과일의 가용성 고형물 함량이 충분히 축적되지 않아 과일의 감미가 떨어지고 수확 이전에 서리 피해를 입으면 후숙 과정에서 부패과 발생률이 높아지며 저장성이 약화된다. 따라서 주산지에서 안정적인 과일 생산을 위해서는 첫서리가 내리기 전에 수확 가능한 품종이 적합할 것으로 판단되며, 본 연구에서 조사된 A.deliciosa 종의 유전자원 중에서는 ‘Garmrok’, ‘SKK33’, ‘Jecy Green’이 녹색 과육 키위프루트에서 조기수확 품종 육성의 모본으로 사용될 것으로 생각된다. A. chinensis 종의 대부분인 황색과육 키위프루트의 경우, 수확 기준이 가용성 고형물 함량의 축적이기도 하지만 가장 중요한 요소는 과육에서의 황색 발현이며, 이들 품종들은 수확기에 가까워지면서 과육의 색이 변하며 황색 발현이 진행되기 때문이다(Montefiori et al., 2009). 후숙 후 안정적인 황색 발현을 위해서는 색차계의 Hue값이 103 미만으로 내려갔을 때 수확하는 것이 적절하다고 판단이 된다. 본 연구에서는 가용성 고형물 함량만을 기준으로 수확하였기 때문에 향후 색 발현을 기준한 수확기 설정이 필요하다.
과중의 범위는 61.3 ‑ 143.2g으로 범위가 커 유용자원 선발에 중요한 지표로 활용될 것이다. 특히, ‘First Emperor’, ‘Kuimi’, ‘Goldone’은 평균 과중이 130g 이상으로 대과 품종을 위한 교배 모본으로 유용할 것으로 판단된다.
키위프루트 유전자원 28점에 대한 후숙 후 과일 특성, 비타민 C, 유기산 함량을 Table 3에 나타내었다. 가용성 고형물 함량은 ‘Hongyang’이 연구에 사용된 자원 중에서 16.8°Brix로 가장 높았고, ‘SKK61’은 14.5°Brix로 A. deliciosa 종의 유전자원 중에서 가장 높았다. ‘Garmrok’은 2013년 육성된 품종으로 가용성 고형물 함량이 18°Brix까지 오르는 것으로 알려져 있으며 Shin et al.(2018)의 연구에서도 외생 에틸렌 처리 후 15와 20°C 저장 조건에서 9일째 18°Brix 이상까지 측정되었다고 언급한 부분에서 본 연구에서 조사된 가용성 고형물 함량과 차이가 있었다. Richardson et al.(1997)의 연구에서 키위프루트의 가용성 고형물은 재배관리에 의한 요인보다 유전적, 기후적 요인에 더 크게 좌우된다고 보고되었다. 위 연구에 비추어 보았을 때, 본 연구에 사용된 ‘Garmrok’은 기후적인 요인과 후숙 조건에서 차이가 있던 것으로 생각된다. 한편 Cheng(2014)은 A. chinensis 집단 내에서 가용성 고형물 함량은 과당과 자당, 산 함량의 수준에 많은 영향을 받으며, 가용성 고형물 함량에 의한 선발은 가용성 고형물 함량의 유전적 향상을 위한 선발에 효과적이라고 보고하였다. 위 결과를 토대로 가용성 고형물 함량이 높은 자원은 고당도 품종 육성에 있어 유용한 자원으로 생각된다. 그러나 가용성 고형물 함량은 과중과 부의 상관관계를 보인다는 보고가 있어 유용자원 선발 시 고려해야 할 부분이다(Cheng, 2014).
Table 3.
Kiwifruit characteristics and organic acid compositions of kiwifruit accessions after ripening
비타민 C의 함량은 25.5 ‑ 165.9mg/100g FW의 큰 범위를 보였는데, 평균 함량은 A. chinensis 유전자원이 A. deliciosa 유전자원에 비해 높았다. Nishiyama et al.(2004)의 연구에 사용된 A. chinensis 유전자원 대부분의 비타민 C 함량은 ‘Hayward’의 함량보다 높았는데, 이 결과는 본 연구의 결과와 일치하였다. A. deliciosa 유전자원의 비타민 C의 함량은 ‘Qinmei’와 ‘SKK33’이 60mg/100g FW 이상의 함량을 보여 녹색 과육 키위프루트에서 비타민 C 함량을 증진시키기 위한 육종 소재로 여겨지며, 연구에 사용된 자원 중 ‘Lushanxiang’과 ‘Redvita’를 비롯해 비타민 C 함량이 100mg/100g FW인 자원은 고 비타민C 함량 품종 육성에 좋은 재료라고 판단된다.
키위프루트의 3가지 유기산을 분석한 결과, A. deliciosa의 유전자원에서 구연산의 함량은 ‘SKK61’이 1.51g/100g FW으로 가장 높았고, 퀸산과 사과산은 모두 ‘Koryoku’에서 가장 높았다. A. chinensis 유전자원의 구연산 함량은 ‘Redvita’에서 가장 높았고, 퀸산 함량은 ‘Haeguem’이, 사과산 함량은 ‘SKK1’이 가장 높았다. Marsh et al.(2004)의 연구에 따르면 퀸산의 비율이 높아지면 바나나향과 같은 감미가 올라가지만 구연산과 사과산은 신맛이 올라가게 하는데, 같은 농도일 경우 사과산이 구연산보다 더 신맛을 많이 낸다고 하였다. 따라서, 사과산의 경우 함량이 높은 자원보다 낮은 자원을 선발하는 것이 적정한 것으로 생각된다.
키위프루트 유전자원 형질의 기초통계량과 변이계수를 Table 4에 나타내었다. 과일의 외형에 있어서는 과중이 가장 높은 변이계수를 보였다. 후숙 후 과실 특성에서는 비타민 C 함량, 퀸산 함량, 적정 산 함량 순으로 높은 변이계수를, 가용성 고형물 함량은 가장 낮은 변이를 보였다. Latocha and Krupa(2007)의 연구에서 비타민 C는 다래나무속의 가장 큰 장점이지만 그 함량은 재배 환경, 수확 후 저장 조건 등에 따라 변이가 크며 연차 간 변이도 크다고 보고되었다. 이에 반해, Nishiyama et al.(2004)의 연구에서는 A. deliciosa, A. chinensis, 그리고 A. arguta를 포함한 Actinidia 과일의 비타민 C 함량은 후숙 과정에서 거의 감소하지 않았으며, 비타민 함량의 차이는 성숙 또는 저장기간의 차이보다 품종 간 차이가 반영된다고 보고하였다. 두 연구에서 상충되는 의견이 있고 유전자원의 비타민 C 함량의 변이를 정확히 파악하기 위해선 다년간 분석이 필요하다고 생각된다.
Table 4.
Basic statistical data for 11 quantitative traits of 28 kiwifruit accessions
다변량 분석
키위 유전자원의 양적 형질 간 상관분석 결과, 대부분의 형질에서 상관관계를 보이지 않았다(Table 5). 과중은 횡경과 r = 0.921의 높은 정의 상관관계를 보여 과중이 종경보다 횡경과 상관관계가 있었다. 비타민 C와 3가지 유기산 사이에는 상관관계가 없었다. Cheng(2014)의 연구에 따르면 가용성 고형물 함량은 2배체 A. chinensis 자원에서 과중과 부의 상관관계(r = ‑ 0.30)를 가진다고 하였다. 본 연구에서도 가용성 고형물 함량은 과중과 r = –0.154의 약한 부의 상관관계를 보였지만 통계적으로 유의하지 않았다. 한편, Li et al.(2010)은 키위프루트의 배수성이 높아질수록 과중과 정의 상관관계를 가진다고 했으며, 과중 이외의 다른 형질(비타민 C 함량, 가용성 고형물 함량, 산 함량)은 상관관계가 없다고 언급하였다. 본 연구에선 배수성을 분석하지 않아 배수성과 형질 간 상관관계를 파악할 수 없었기에 추가 연구가 필요할 것으로 판단된다.
Table 5.
Correlation coefficients among 11 quantitative traits
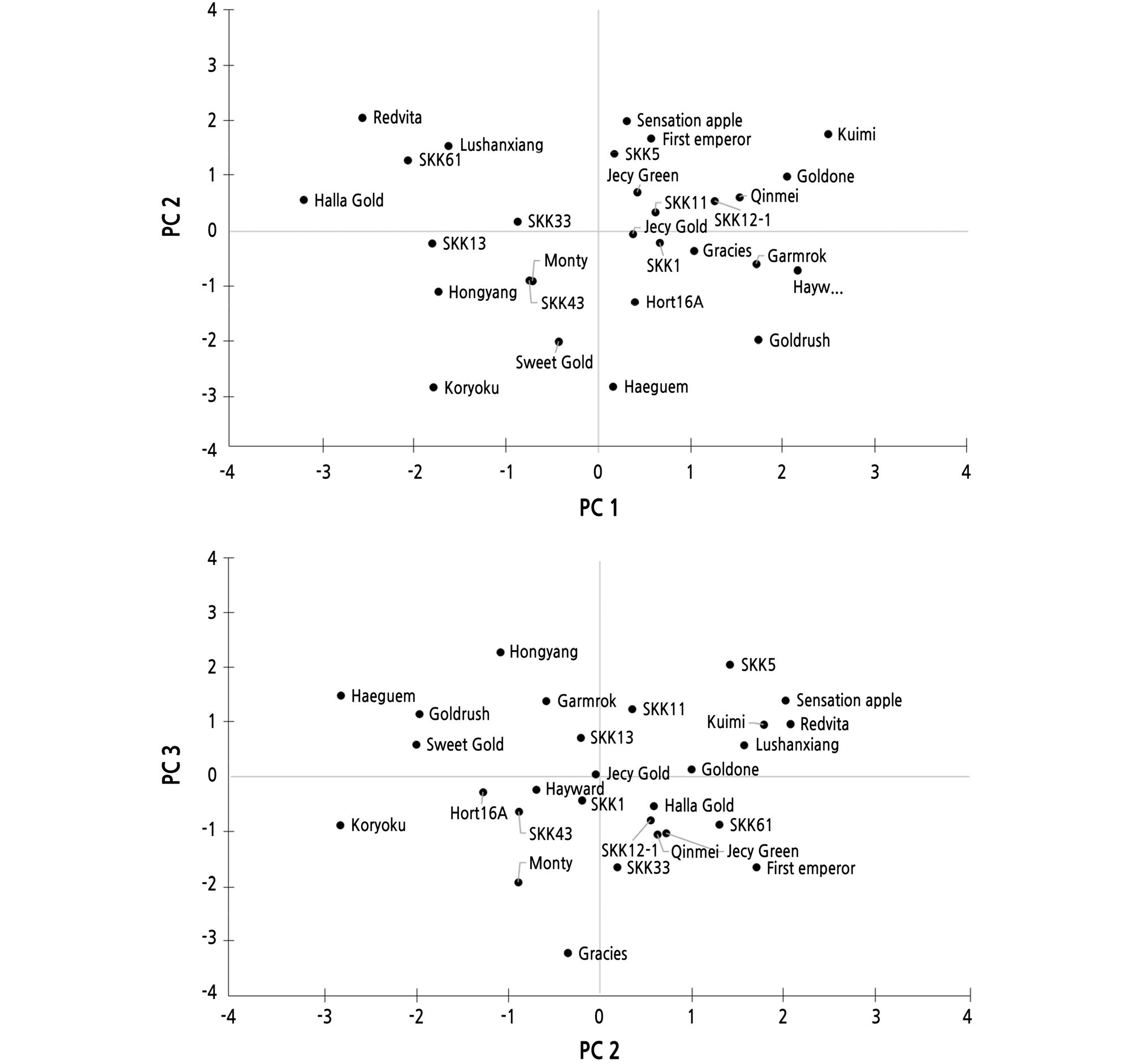
Lee et al.(2017)의 주성분분석 방법을 참고하여 키위프루트 유전자원의 11가지 양적 형질에 대한 주성분분석으로 획득한 고유값과 설명비율은 Table 6과 같다. 분석에 이용된 11개의 양적 형질 중 고유값과 설명비율을 고려했을 때, 제5주성분까지 1개 이상의 형질을 대표할 수 있었으며 나머지 6개의 주성분은 1가지 이상의 형질을 대표할 수 없었다. 5개의 주성분과 양적 형질 간 상관분석을 실시하였다(Table 7). 제1주성분은 과중과 횡경의 순서로 높은 정의 상관관계를 나타내어 과실의 외형으로 정의할 수 있었다. 제2주성분은 구연산과 비타민 C 함량으로 정의하였고, 제3주성분은 가용성 고형물 함량으로 정의하였다. 제1 및 2주성분을 점수로 산점도를 그렸을 때, 제1사분면에는 과중이 큰 유전자원들이 분포하였고 제2사분면에는 비타민 C 함량이 높은 유전자원이 분포함을 알 수 있었다(Fig. 1). 마찬가지로 제2 및 3주성분을 동일하게 나타냈을 때, 제2사분면은 가용성 고형물 함량이 높은 유전자원이 분포하였다(Fig. 1). 주성분 분석의 결과는 키위프루트 유전자원의 여러 형질을 5가지로 압축시켰으며 우선순위를 설정하게 하였다. 따라서 압축된 변량을 이용해 유전자원을 분류하고 평가하며 육종 프로그램에서 계통 선발에 있어 유용한 지표로 사용될 것이며 이외의 형질 조사에 드는 노력을 절감시킬 것이다.
Table 6.
Eigenvalues and proportions of principal component of 11 quantitative traits of kiwifruit germplasms
Table 7.
Five principal components among quantitative traits of kiwifruit germplasm
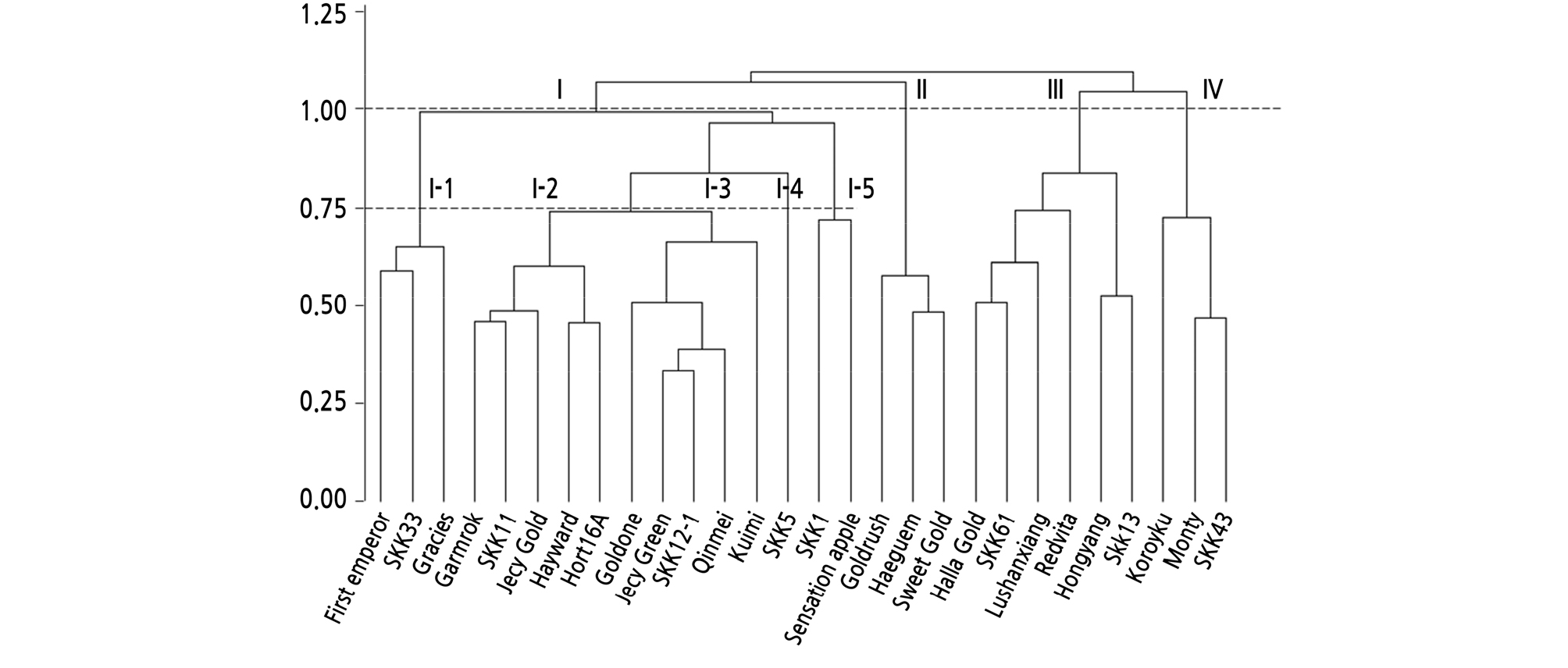
5개의 주성분에 기초해 군집분석 결과, 28개의 키위프루트 유전자원은 1.0의 평균거리를 기준으로 4개의 군집으로 나누어졌고 제1군집은 0.75의 평균거리를 기준으로 5개의 소분류군으로 구분할 수 있었다(Fig. 2). 나누어진 유전자원은 원산지와 계통간의 구별이 없었다(Table 1, Fig. 2). 4개의 군집 중, 평균 과중은 제1군집이 가장 높았고, 가용성 고형물 함량은 제2군집이, 비타민 C 함량은 제4군집이 가장 높았다. 키위프루트는 수확 시 0.9 ‑ 2.5%의 총 유기산을 함유하는데 구연산이 40 ‑ 50%, 퀸산이 40 ‑ 50%, 그리고 사과산이 10% 비율로 분포한다. 그 맛에는 당과 산의 비율이 영향을 주지만 3가지 유기산 함량의 비율도 영향을 미친다(Marsh et al., 2004). 위 연구를 기준으로 하여 4개 군집의 3가지 유기산(구연산, 퀸산, 사과산) 함량을 비율로 나타냈을 때, 제1 군집이 각각 56.3, 26.5, 17.2%이며, 제2군집은 67.1, 46.8, 16.1%, 제3군집은 47.2, 34.0, 18.8%, 제4군집은 58.3, 24.2, 17.5%이다.
군집분석은 육종가에게 큰 규모의 유전자원에서 효율적으로 목표하는 형질의 자원을 선발하게 한다(Lee et al., 2017). 본 연구의 데이터를 토대로 육종가가 고당도 대과 품종을 육성하고자 한다면 제1군집과 제3군집에서 유용한 자원을 찾을 것이고 비타민 C 함량이 높은 품종을 육성하고자 한다면 제4군집의 자원을 교배모본으로 사용하는 것이 가장 적절할 것이다. 만약 육종가가 Marsh et al.(2004)의 연구를 토대로 유기산의 적정 비율을 목표로 선발한다면 퀸산의 비율이 가장 높은 제2군집에서 유용자원을 선발할 것이다.
이상의 결과를 종합하면 다변량 분석을 이용한 키위프루트 유전자원 특성 평가 결과는 기능성이 높고, 소비 트렌드를 반영한 다양한 품종 육성을 위한 기초자료로 활용될 수 있을 것으로 판단된다.