서 언
재료 및 방법
식물 재배
접종원 준비
병원균 접종 및 병조사
통계 분석
결과 및 고찰
병리검정 조건 확립을 위한 배추 품종 선발
배추의 생육 정도에 따른 검은썩음병 발생
접종원 농도에 따른 배추 검은썩음병 발생
습실처리 기간에 따른 배추 검은썩음병 발생
습실처리 온도에 따른 배추 검은썩음병 발생
서 언
Pammel(1895)이 1895년 미국 아이오와주에서 처음 보고한 검은썩음병(black rot)은 평균 기온이 25 ‑ 30°C인 다습한 지역에서 재배하고 있는 배추, 양배추, 꽃양배추, 콜라비, 무 등의 배추과 작물에 발생하여 경제적으로 큰 손실을 가져오는 중요한 병해이다(Jorgensen and Walter, 1955; Williams, 1980). 이 병은 기본적으로 종자 전염 병해이나 감염된 식물, 감염된 토양 및 이병 잔재물 등을 통해 전염하기도 한다(Cook et al., 1952; Walker, 1953; Schaad and Alvarez, 1993). 이 병에 감염된 배추는 잎의 가장자리가 노랗게 변하고, 엽맥이 흑색으로 변한다. 병이 진전되면 옅은 노랑색의 부정형 반점이 나타나며 주맥은 퇴록하고, 엽맥과 줄기의 유관속 조직이 괴사하거나 검게 변하며, 잎이 검은 갈색으로 변하면서 식물체가 시들거나 고사하기도 한다. 그리고 이병엽에 2차적으로 Erwinia속과 Pseudomonas속의 병원균이 감염하게 되면 무름병 증상을 나타내기도 한다(Cook et al., 1952; Williams, 1980).
배추과 작물의 검은썩음병은 Xanthomonas campestris pv. campestris(Xcc)에 의해 발생하는데, 이 병원균은5 ‑ 38°C에서 생존이 가능하며, 포자를 형성하지 않는 그람 음성균이다. Vincente et al.(2001)은 배추과 작물의 저항성 판별 기주 5개[‘Miracle F1’ cauliflower(Brassica oleraceae), ‘Florida Broad leaf’ mustard(Brassica juncea), ‘PI 199947’ Ethiopian mustard(Brassica carinata), ‘Seven Top’ turnip(Brassica rapa), ‘Just Right Hybrid’ turnip(B. rapa)]와 감수성 품종[‘Wirosa F1’ Savoy cabbage(B. oleraceae)] 1개를 사용하여 Xcc 균주들을 6개의 race로 구분하였다. 이들 저항성 판별 기주는 단인자 우성 저항성 유전자인 R1, R3, R4를 보유하고 있으며, 배추과 작물의 Xcc에 대한 저항성은 유전자대유전자 가설(gene for gene theory)로 설명할 수 있다고 하였다(Vincente et al., 2002, Vincente and Holub, 2013). 하지만 이들 race 판별기주는 대부분 계통이 아니고 품종이어서 다른 나라의 연구자들은 이들 판별품종을 확보하지 못하여 분리한 Xcc 균주들의 race를 동정하는 데 어려움을 겪고 있다. Xcc 균주들은 세계적으로 race 1과 race 4가 우점하는 것으로 알려져 있다(Vincente and Holub, 2013).
Xcc 병원균은 빗방울과 바람, 물에 의해 전반 되고, 일반적으로 잎 가장자리의 수공을 통해 식물체 내부로 침입하고 물관을 통해 이동한다(Russell, 1898; Cook et al., 1952; Vincente and Holub, 2013). 그리고 기온이 25°C로 지속될 경우 xanthan이라고 하는 다당류를 분비하여 식물체내 물관에서 수분의 흐름을 막아 검은썩음병을 야기한다(Paul, 1980). 한편 종자전염병균인 Xcc는 이병종자에서 3년 동안 생존이 가능한데, 토양에서도 기주없이 여름에는 20일, 그리고 겨울에는 40일 동안 생존할 수 있다(Clayton, 1924; Walker, 1941; Schaad and White, 1974; Dane and Shaw, 1996). 하지만 토양에서 세균만으로 존재하는 것보다 이병식물 잔재물에 있을 때 더 오래 생존할 수 있다(Arias et al., 2000).
배추과 작물의 검은썩음병을 방제하기 위하여 윤작을 하거나 종자에 물리화학적 처리를 하여 제조한 무균 종자를 재배하는 것이 비교적 효과적이다(Gangopadhyay and Gill, 1977; McKeen, 1981; Kishun, 1984; Schultz and Gabrielson, 1986; Schaad and Alvarez, 1993). 또한 보르도액과 항생제 등을 이용한 화학적 방제(Knosel, 1965; Onsando, 1988; Gupta, 1991; Bhat et al., 2000), 길항미생물 Bacillus 균주 배양액을 이용한 생물학적 방제 즉, 식물체의 뿌리를 미생물 배양액에 침지한 후 이식하거나, 배양액을 종자에 침지하여 파종하기 및 배양액을 엽면에 살포하여 검은썩음병을 방제하는 연구가 진행되고 있다(Jalali and Parashar, 1995; Pichard and Thouvenot, 1999; Wulff et al., 2002). 하지만 우리나라의 기후가 점점 아열대 기후로 변하면서 검은썩음병 발생도 크게 증가하고 있어(personal communication), 이들 방법을 통한 실질적인 방제효과를 얻기는 매우 어려운 현실이다.
일반적으로 저항성 품종을 재배하여 식물병, 특히 토양병, 세균병 및 바이러스병을 방제하는 것은 친환경적이면서도 가장 효과적인 방제 방법으로 인식되고 있다(Taylor et al., 2002; Lee et al., 2018; Vijeth et al., 2018; Yerasu et al., 2019). 하지만 우리나라에서 Xcc에 대한 저항성으로 공시하고 판매하는 배추 품종은 아직 없으며, 배추 검은썩음병에 관한 연구도 매우 적다. 저항성 품종을 육성하기 위해서는 Xcc에 대한 저항성 유전자원의 선발, 그리고 저항성 유전자원과의 교배에서 생긴 대량의 종자들로부터 저항성 개체를 효과적으로 선발하는 것이 필수적이다. 하지만, 배추 검은썩음병에 대한 효과적인 저항성 검정 방법 개발에 관한 보고는 거의 없다.
본 연구에서는 효율적인 배추 검은썩음병 저항성 검정법을 확립하기 위하여, 시판하고 있는 배추 품종 88종의 Xcc에 대한 저항성을 조사하고, 검은썩음병에 대한 저항성 정도에 차이가 있는 6개 품종을 선발하였다. 그리고 이들 품종의 생육 정도, 접종하는 Xcc의 농도, 병원균 접종 후 습실상의 온도와 습실처리 기간 등의 다양한 발병 조건에 따른 배추 검은썩음병 발생 정도를 조사하였다.
재료 및 방법
식물 재배
시판되고 있는 배추 88개 품종(신젠타종묘로부터 ‘가을황’, ‘신농봄’, ‘CR일사천리’, ‘아름찬’, ‘올품’, ‘황금알’, ‘CR농심’, ‘CR안심’, ‘CR진심’ 및 ‘CR황금’을, 몬산토코리아로부터 ‘강력여름’, ‘노랑관동’, ‘노랑김장’, ‘노랑김치’, ‘노랑추석’, ‘부활’, ‘불암3호’, ‘불암여름배추’, ‘불암플러스’, ‘삼보엇갈이’, ‘썬그린’, ‘진청’, ‘참이슬엇갈이’, ‘챔피온’ 및 ‘CR청록’을, 농우바이오로부터 ‘금방울’, ‘대통’, ‘뚝심엇갈이’, ‘맞춤’, ‘산울림’, ‘쌈이랑’, ‘우리’, ‘월동천하’, ‘추월’, ‘CR맛’, ‘CR여름맛’, ‘CR입춘’, ‘CR하계’ 및 ‘월동대장’을, 팜한농으로부터 ‘CR알찬’과 ‘CR맛짱’을, 코레곤종묘에서 ‘CR요시마사’, ‘CR키요시’, ‘CR황록’ 및 ‘금촌얼갈이’를, 현대종묘로부터 ‘씨알제왕’, ‘CR고냉지노랑’ 및 ‘CR황태자’를, 제일종묘로부터 ‘CR명가’를, 사카타코리아로부터 ‘노랑맛하장’, ‘파워춘광’, ‘춘광’, ‘옥황씨알’, ‘상장군’, ‘영광’, ‘태봉’, ‘천하장군’, ‘하대장군’, ‘CR명품’, ‘CR장군’, ‘탐이나쌈’, ‘CR미락쌈’, ‘겨울진명’, ‘월동장군’, ‘겨울장군’ 및 ‘CR새신록엇갈이’를, 농협종묘로부터 ‘CR강산’을, 우리종묘로부터 ‘청옥’과 ‘청야’를, 제일종묘로부터 ‘항암쌈배추’를, 다끼이종묘에서 ‘CR하루요시’를, 그리고 아시아종묘로부터 ‘가을속노랑’, ‘노랑미니배추’, ‘봄노랑’, ‘춘쌈황51’, ‘장생3호’, ‘춘연’, ‘휘모리’, ‘만수무강’, ‘조은여름’, ‘CR설춘’, ‘CR하광’ 및 ‘춘쌈황51’을, 중국 Changxing Seed로부터 ‘Jinjinsanhaodabaicai’를, 중국 Degao Seed로부터 ‘DegaoCR1016’와 ‘DegaoCR117’을, 일본 Norin으로부터 ‘Akimeki’, ‘Kien80’ 및 ‘CR Kanki NO.100’를, 일본 Takayama Seed로부터 ‘CRgokigen90’을 구입하여 실험에 사용하였다.
발병 조건에 따른 배추 품종들의 검은썩음병 발생 실험은, 88개의 시판 배추 품종의 Xcc에 대한 저항성 정도를 조사한 결과를 토대로 배추 검은썩음병에 대하여 저항성 정도가 서로 다른 여섯 품종(‘만수무강’, ‘월동천하’, ‘CR안심’ ‘불암3호’, ‘춘광’ 및 ‘CR농심’)을 실험에 사용하였다.
생육 정도에 따른 배추 검은썩음병 발생 실험을 제외한 모든 실험에 사용한 식물체는 5×8 육묘용 연결포트(70mL/pot, Bumnong, Jeongup, Korea)에 원예용상토 5호(Punong, Gyeongju, Korea)를 넣고 포트당 2립씩 파종한 뒤 온실(25 ± 5°C)에서 재배하였다. 파종 6일 후에 포트당 1개의 식물체가 되도록 배추를 솎아주거나 이식해주었고, 파종 10일 후 2엽이 전개된 유묘를 실험에 사용하였다. 그리고 생육 정도에 따른 배추 검은썩음병 발생 정도를 조사하기 위해서는 위와 동일한 방법으로 파종하고 온실(25 ± 5°C)에서 9일, 10일, 11일, 12일, 13일, 14일 동안 재배한 유묘를 실험에 사용하였다(Fig. 1).
접종원 준비
배추 검은썩음병균인XccKACC 10377 균주를 농촌진흥청 농업유전자원센터(KACC, Rural Development Administration, Jeonju, Korea)로부터 분양 받아 사용하였다. 그리고 병원균의 장기 보관을 위하여 20% glycerol에 현탁하여 ‑ 70°C deep freezer에 저장해두고 실험할 때 하나씩 꺼내어 실험에 사용하였다. 병원균을 tryptic soy agar(TSA; Becton, Dickinson and Co., Sparks, MD, USA) 배지에 접종하여 30°C에서 1일간 전배양하고, 이를 새로운 TSA 배지에 다시 평판도말하여 30°C에서 2일간 배양하였다. 배양한 XccKACC 10377 균주에 멸균수를 5 mL 넣고 병원균을 수확하고, 수확한 세균 pellet에 멸균수를 넣고 잘 흔들어 현탁한 후에 UV spectrophotometer(Beckman Coulter Inc., Brea, CA, USA)를 사용하여 흡광도(OD, optical density)를 측정하였다. 세균 현탁액의 밀도를 OD600 = 0.1757(1.0 × 108cfu/mL)가 되도록 멸균수를 이용하여 조정한 뒤 접종원으로 사용하였다.
병원균 농도에 따른 배추 검은썩음병 발생을 조사하기 위하여, 병원균의 농도가 1.0 × 105, 1.0 × 106, 1.0 × 107, 1.0 × 108 cfu/mL이 되도록 병원균의 OD600값을 각각 0.0066, 0.0197, 0.0589, 0.1757이 되도록 조정한 세균 현탁액을 실험에 사용하였다.
병원균 접종 및 병조사
준비한 Xcc KACC 10377 균주의 세균 현탁액을 식물체 잎 앞, 뒷면에 모두 병원균이 접종될 수 있도록 스프레이로 분무접종하였다. 병원균을 접종한 식물체는 28°C 습실상에서 암상태에서 48시간 동안 습실처리한 후에 식물체를 항온항습실(25°C, 상대습도 80%)로 이동하여 하루에 12시간씩 광(PPFD 55µmol·m-2·s-1)을 조사하면서 재배하였다.
습실처리 온도에 따른 배추 검은썩음병 발생 실험은 접종한 식물체를 각각 20°C, 25°C, 28°C 및 30°C의 습실상에서 암상태로 48시간 습실처리한 후에 항온항습실(25°C, 상대습도 80%)로 이동하여 하루에 12시간씩 광(55µmol·m-2·s-1)을 조사하면서 재배하였다.
또한 습실처리 기간에 따른 배추 검은썩음병 발생 정도를 비교하기 위하여, 접종한 식물체를 28°C 습실상에서 각각 24시간, 48시간 및 72시간 동안 습실처리 한 후에 항온항습실(25°C, 상대습도 80%)로 이동하여 하루에 12시간씩 광(55µmol·m-2·s-1)을 조사하면서 재배하였다.
접종 6일 후 배추 잎에 발생한 검은썩음병 병반의 면적률(%), 즉 전체 잎 면적 중 병반이차지하는 면적의 비율(%)을 달관조사하고, 평균 병반면적률(%)을 계산하였다.
통계 분석
모든 실험은 처리 당 10개 식물체를 접종하였으며 실험은 2회 반복 수행하였으며, 이들 결과는 SAS 프로그램(SAS 9.1, SAS Institute Inc., Cary, NC)을 이용하여 ANOVA 분석을 하고, 처리 평균 간 비교를 위하여 Duncan’s multiple range test(p = 0.05)를 실시하였다
결과 및 고찰
병리검정 조건 확립을 위한 배추 품종 선발
시판 배추 품종 88개의 Xcc KACC 10377에 대한 저항성을 실험한 결과, 실험한 품종 중 23개(26%)는 5% 이하의 낮은 병반면적률을 보여 이들은 고도의 저항성 품종임을 알 수 있었다(Table 1). 그리고 22개(25%)는 5.1 ‑ 10%의 병반면적률을 나타내 실험한 품종 중 약 51%는 10% 이하의 검은썩은병 병반면적률을 나타냈다. 실험한 품종 중 20% 이상의 병반면적률을 보이는 품종은 26개(30%)였으며, 이중 7개 품종은 69% 이상의 높은 감수성을 나타냈다. 고도 감수성 품종 중 2개는 일본 품종이었으며, 나머지 품종들은 ‘CR 농심’, ‘장생3호’, ‘불암3호’, ‘춘광’ 및 ‘춘연’이었다. 이들 중 ‘춘광’은 강원도 배추 주산지에 널리 재배하고 있는 품종인데, 최근 3년 동안 강원도 배추 주산지에서 검은썩음병이 심하게 발생하였는데, 이것은 기후 온난화와 이 품종의 검은썩음병에 대한 높은 감수성 때문으로 생각되었다. 따라서 우리나라 기후도 점차 온난화됨에 따라 배추의 검은썩음병 발생이 증가하고 있기 때문에 Xcc에 대하여 높은 감수성을 나타내는 배추 품종들의 재배를 회피하는 것이 바람직할 것이다.
Table 1.
Resistance degree of 88 commercial Chinese cabbage cultivars to Xanthomonas campestris pv. campestris KACC 10377z
zTen-day-old seedlings of Chinese cabbage cultivars were inoculated with a bacterial suspension (1.0 × 108 cfu/mL) of Xanthomonas campestris pv. campestris KACC 10377 by spray method. The inoculated plants were incubated in a humidity chamber at 28°C for 48 hour and then transferred to a growth chamber at 25°C and RH 80% with 12-hour light a day. Six days after inoculation, the percent diseased leaf area of each plant was scored.
실험에 사용한 품종 중 종자회사에서 검은썩음병에 대한 저항성으로 공시한 품종은 없었지만, 88종 품종 배추의 검은썩음병에 대한 저항성 정도를 실험한 결과(Table 1)에서 1% 이하의 병반면적률을 나타낸 3개 품종(‘만수무강’, ‘월동천하’, ‘CR안심’)과 70% 이상의 병반면적률을 나타낸 3개 품종(‘불암3호’, ‘춘광’, ‘CR농심’)을 배추 검은썩음병 저항성 검정 체계 확립을 위한 실험에 사용하기 위하여 선발하였다.
배추의 생육 정도에 따른 검은썩음병 발생
저항성 품종을 개발하기 위한 병리검정은 유묘의 생육 시기가 빠를수록, 그리고 저항성과 감수성 차이가 뚜렷하게 나타나는 식물체의 생육 시기에 병원균을 접종하는 것이 효과적이다. 저항성 품종으로 선발한 3개 품종(‘만수무강’, ‘월동천하’, ‘CR안심’)과 감수성 품종으로 선발한 3개 품종(‘불암3호’, ‘춘광’, ‘CR농심’)의 배추를 파종하고 온실에서 9일, 10일, 11일, 12일, 13일, 14일 동안 재배한 후에 검은썩음병균을 접종한 결과, 저항성 3개 품종들은 배추 생육 기간에 따라 각각 1.5%, 0.0%, 0.1%, 0.3%, 2.5%, 9.4%의 병반면적률을 보였다(Fig. 2). 따라서 실험한 저항성 품종들은 재배 기간이 증가함에 따라 이들 품종의 저항성이 다소 감소하는 경향을 나타낸다는 것을 알 수 있었다. 그리고 감수성 3개 품종은 파종하고 온실에서 9일, 10일, 11일, 12일, 13일, 14일 동안 재배한 유묘에 검은썩음병균을 접종하였을 때, 재배 기간에 따라 각각 38.1%, 48.8%, 46.4%, 37.1%, 34.4%, 38.1%의 병반면적률을 나타내었다(Fig. 2). 감수성 품종들은 재배 기간에 따라 큰 차이를 나타내지 않았으나, 실험한 생육 시기 중 파종 10일 후의 배추들이 Xcc에 대하여 감수성이 가장 높고 그 다음은 파종 11일 후 유묘라는 것을 알 수 있었다.
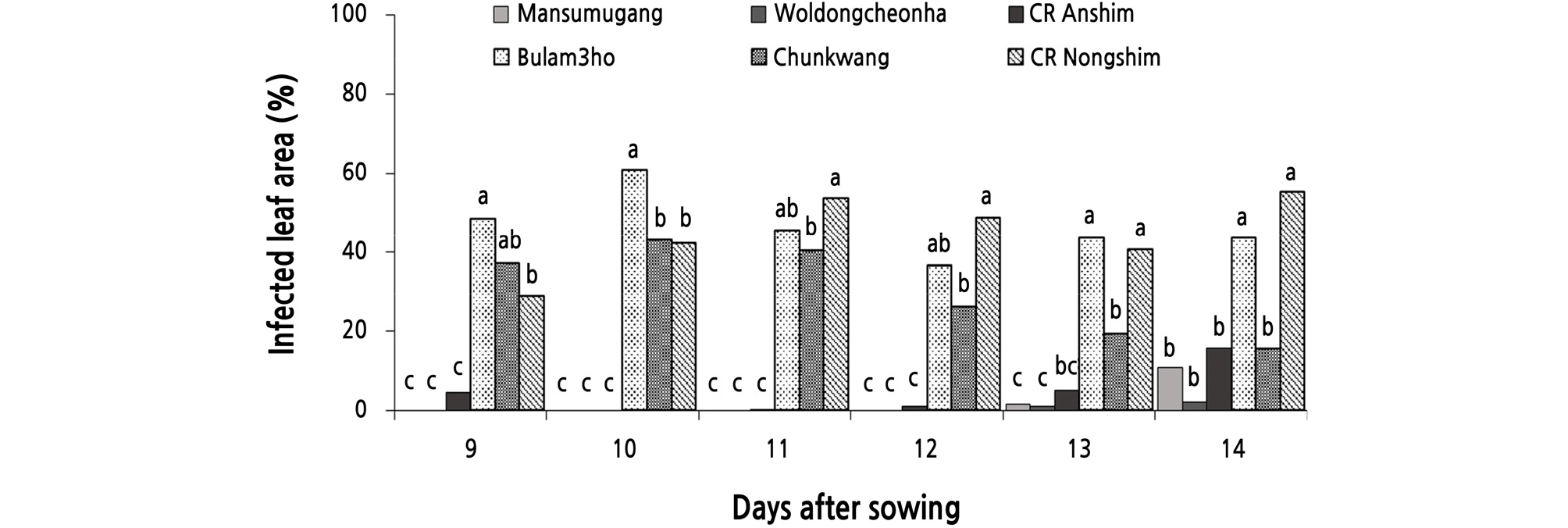
Fig. 2.
Development of black rot on six cultivars of Chinese cabbage at different plant growth stage. Nine-, ten-, eleven-, twelve-, thirteen-, and fourteen-day-old seedlings of each cultivar were inoculated with a bacterial suspension (1.0 × 108 cfu/mL) of Xanthomonas campestris pv. campestris KACC 10377 by spray method. The inoculated plants were incubated in a humidity chamber at 28°C for 48 hour and then transferred to a growth room at 25°C and 80% RH with 12-hour light a day. Six days after inoculation, disease severity was measured and represented as percentage of infected leaf area. The data were obtained from ten replicates with two repetitions.Values labeled with the same letter within each growth stage are not significantly different based on Duncan’s multiple range test at p = 0.05.
Doullah et al.(2006)은 Alternaria brassicicola에 의한 무 검은무늬병의 경우에 어린 잎보다 오래된 잎이 감수성이 크다고 하였으며, Lee et al.(2017)은 파종하고 온실에서 10 ‑ 19일 동안 재배한 유묘에 A. brassicicola를 접종하였을 때 생육 기간이 길수록 검은무늬병 발생이 적었다고 하였다. 한편, Lee et al.(2013)은 양배추 검은썩음병의 경우 핀셋 접종법으로 접종하였을 때 양배추의 생장 기간이 길수록 Xcc에 대한 감수성이 증가한다고 보고하였다. 따라서 유묘의 생육 정도에 따른 식물병 발생은 작물에 따라 병해 종류에 따라 다르다고 생각되었다.
그리고 본 연구에서는 파종 후 9, 10, 11, 12일 동안 재배한 유묘들은 감수성과 저항성 품종간의 평균 병반면적률의 차이가 통계적으로 유의성 있게 나타났다. 이들 재배 기간 중 파종 10일 후 유묘에서는 감수성으로 선발한 품종 중 ‘불암3호’, ‘춘광’, ‘CR농심’의 경우에 각각 61.0, 43.0%, 42.3%의 병반면적률을 보였으나, 저항성 품종으로 선발한 3개 품종 모두에서 검은썩음병이 발생하지 않았다(Fig. 2). 따라서 감수성 품종과 저항성 품종 간의 병반면적률 차이가 가장 커서 품종의 저항성 및 감수성 특성을 가장 잘 나타낼 수 있는 재배 기간인 파종 10일 후 유묘(2엽 완전전개)를 사용하는 것이 배추 검은썩음병 저항성 검정에 효과적인 것으로 생각되었다.
접종원 농도에 따른 배추 검은썩음병 발생
검은썩음병에 대하여 저항성인 3개 품종과 감수성인 3개 품종에 Xcc를 1.0 × 105, 1.0 × 106, 1.0 × 107, 1.0 × 108cfu/mL로 접종하고 검은썩음병 발생을 조사한 결과, 저항성 품종들의 평균 병반면적률(%)은 각각 0.3, 0.0, 0.8, 1.5% 였으며, 감수성 품종들의 평균 병반면적률(%)은 각각 19.7, 38.3, 59.7, 72.5%를 보였다(Fig. 3). 이들 결과로부터, 실험한 감수성 품종들은 접종 농도가 1.0 × 105cfu/mL에서 1.0 × 108cfu/mL로 접종 농도가 증가함에 따라 농도의존적으로 병반면적률이 크게 증가하나, 실험한 저항성 품종들은 실험한 농도에서 저항성에 거의 변화가 없다는 것을 알 수 있었다.
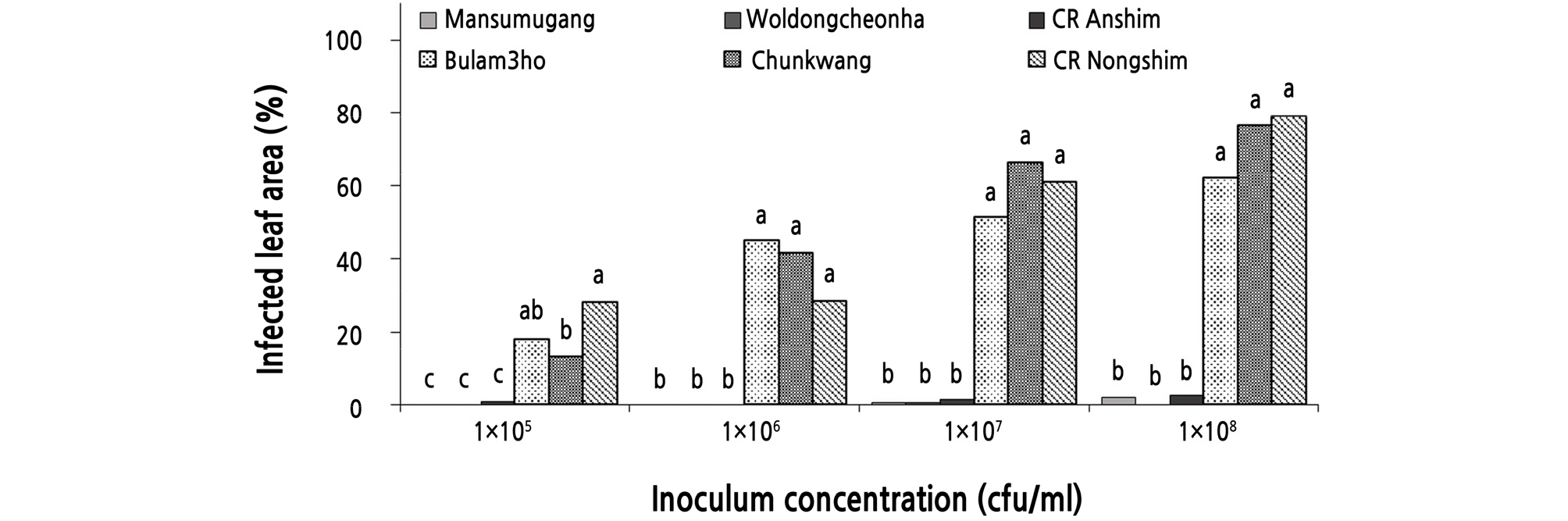
Fig. 3.
Effects of inoculum concentration on the development of black rot on six cultivars of Chinese cabbage. Ten-day-old seedlings of each cultivar were inoculated with Xanthomonas campestris pv. campestris KACC 10377 by spraying a bacterial suspension at concentrations of 1.0 × 105, 1.0 × 106, 1.0 × 107, and 1.0 × 108 cfu/mL. The inoculated plants were incubated in a humidity chamber at 28°C for 48 hour and then transferred to a growth room at 25°C and 80% RH with 12-hour light a day. Six days after inoculation, disease severity was measured and represented as percentage of infected leaf area. The data were obtained from ten replicates with two repetitions.Values labeled with the same letter within each inoculum concentration are not significantly different based on Duncan’s multiple range test at p = 0.05.
뿌리혹병균(Plasmodiophra brassicae)에 대한 배추의 저항성(James and Williams, 1980; Yoshikawa, 1993; Kuginuki et al., 1999), 시들음병균(Fusarium oxysporum f. sp. lycopersici)에 대한 토마토의 저항성(McGrath et al., 1987; Scott and Jones, 1989; Bournival and Vallejos, 1991) 및 덩굴쪼김병(Fusarium oxysporum f. sp. melonis)에 대한 멜론의 저항성(Messiaen et al., 1962; Risser et al., 1976) 등은 질적 저항성으로 알려져 있는데, 이 저항성의 특징은 접종원의 농도가 증가하여도 저항성 품종의 병 발생에 차이가 없고, 병원균의 race에 따라 병 발생에 변화를 나타낸다고 알려져 있다(Lee et al., 2015; Kim et al., 2016). 이와 달리 양적 저항성의 경우에는 접종 농도가 증가하면 저항성 정도가 낮아지는 경우가 많다. 예를 들면, 고추 역병의 경우에는 단일 농도(5.0 × 104 sporangia/pot)로 접종하였을 때 고추 100개 품종 중 6개 품종은 병원력(virulence)가 다른 4개 역병균 모두에 대해 고도의 저항성을 나타내었는데, 이들 품종도 더 높은 농도로 접종하였을 경우, 접종 농도가 증가함에 따라 병 발생이 증가하였다(Jo et al., 2014). 고추 풋마름병의 경우에도 역시 단일농도로 접종하였을 때, 고도의 저항성을 나타내었던 품종도 접종하는 병원균 농도에 따라 풋마름병 저항성 차이를 보였다(Hwang et al., 2017). 하지만 본 연구의 배추 검은썩음병의 경우에는 실험한 저항성 품종에서 접종하는 병원균의 농도가 증가하여도 병 저항성에 거의 차이를 나타내지 않는 질적 저항성의 특징을 나타냈다. 하지만 지금까지 배추의 검은썩음병에 대한 배추의 저항성이 질적 저항성이라는 보고는 없으므로, 더 많은 실험을 통해 확인할 필요가 있다.
실험한 모든 접종 농도에서 저항성 품종 그룹과 감수성 품종 그룹 간에 통계적으로 유의성 있는 차이를 보였으나, 실험 한 접종 농도 중 1.0 × 108cfu/mL로 접종하였을 때 저항성 품종으로 선발한 ‘만수무강’, ‘월동천하’, ‘CR안심’의 병반면적률(%)은 각각 2.0, 0.0, 2.5%이었고, 감수성 품종으로 선발한 ‘불암3호’, ‘춘광’, ‘CR농심’의 병반면적률(%)은 각각 62.0, 76.5, 79.0%으로 각 그룹의 품종 간에 통계적인 유의차가 없으며 두 그룹 간에는 가장 높은 통계적으로 유의성 있는 차이를 보였다(Fig. 3). 따라서 배추의 검은썩음병 저항성 검정을 위해 Xcc 세균현탁액을 1.0 × 108cfu/mL로 접종하는 것이 효과적이라고 생각되었다. 하지만 KACC 10377가 아닌 다른 Xcc 균주를 사용하여 실험할 때는 균주 병원력(virulence)에 따라 접종 농도를 달리할 필요가 있을 것으로 생각된다. 즉, 사용하는 균주의 병원력이 KACC 10377보다 강하면 접종하는 세균 농도를 낮추어 주고, 병원력이 약하면 1.0 × 108cfu/mL 보다 접종원 농도를 높여야 할 것이다.
습실처리 기간에 따른 배추 검은썩음병 발생
선발한 6개 품종의 배추 유묘에 검은썩음병균 Xcc를 접종하고 접종한 식물체를 28°C 습실상에서 각각 24, 48, 72시간 습실처리한 후 항온항습실(25°C, 상대습도 80%)로 이동하여 하루에 12시간씩 광을 조사하고 저면관수하며 검은썩음병 발생을 조사한 결과, 접종한 식물을 48시간 동안 습실처리한 경우에 6개 품종 ‘만수무강’, ‘월동천하’, ‘CR안심’, ‘불암3호’, ‘춘광’, ‘CR농심’의 평균 검은썩음병 병반면적률은 각각 0.0, 0.0, 1.5, 63.5, 47.0, 48.3%을 나타냈다. 저항성 선발 3개 품종은 0.5%의 평균 병반면적률을 그리고 감수성 품종들의 평균 병반면적률은 52.9%로 두 그룹 간에 유의성 있는 차이를 보였다(Fig. 4).
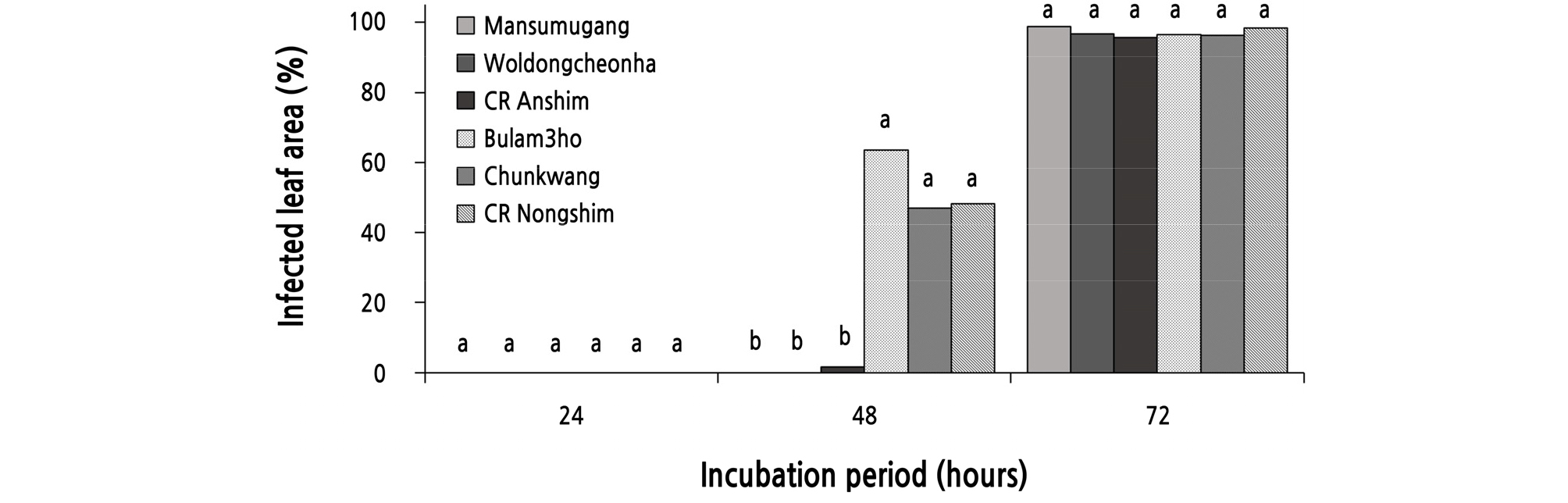
Fig. 4.
Development of black rot on six cultivars of Chinese cabbage according to incubation period in a humidity chamber. Ten-day-old seedlings of each cultivar were inoculated with a bacterial suspension (1.0 × 108 cfu/mL) of Xanthomonas campestris pv. campestris KACC 10377 by spray method. The inoculated plants were incubated in a dew chamber at 28°C for 24, 48, and 72 hours and then transferred to a growth room at 25°C and 80% RH with 12-hour light a day. Six days after inoculation, disease severity was measured and represented as percentage of infected leaf area. The data were obtained from ten replicates with two repetitions.Values labeled with the same letter within each incubation period are not significantly different based on Duncan’s multiple range test at p = 0.05.
한편 24시간 동안 습실상에서 식물체를 재배한 경우에는 실험한 모든 품종들에서 검은썩음병이 발생하지 않았으며, 72시간 동안 습실처리하였을 때에는 선발한 6개 품종은 저항성을 나타내는 품종없이 모두 95% 이상의 병반면적률(%)을 보였다(Fig. 4). 하지만 자연상태에서 72시간 동안 95% 이상의 포화습도가 유지되는 경우는 거의 없어 이와 같은 요인으로 자연상태에서 저항성 품종의 저항성이 무너지는 일은 거의 없을 것으로 생각된다. 따라서 검은썩음병에 대한 배추의 저항성 정도를 조사하기 위해서는 배추 유묘에 병원균을 접종하고 습실상에서 48시간 동안 습실처리하는 것이 효과적이라고 생각되었다.
습실처리 온도에 따른 배추 검은썩음병 발생
선발한 6개 품종의 배추 유묘에 검은썩음병균을 접종한 후 20, 25, 28, 30°C에서 48시간 동안 습실처리한 후에 항온항습실(25°C, 상대습도 80%)에서 재배하여 검은썩음병 발생을 조사한 결과, 감수성 3개 품종들은 28°C와 30°C에서 습실처리 하였을 때에는 각각 50.0%와 72.8%의 평균 병반면적률(%)을 보였다(Fig. 5). 하지만 Xcc를 접종하고 20°C와 25°C에서 습실처리하였을 때에는 모든 품종에서 검은썩음병이 거의 발생하지 않았다. 따라서 감수성 품종은 Xcc 병원균을 배추 유묘에 접종하고 30°C에서 습실처리하는 것이 28°C에서 습실처리하는 것보다 검은썩음병이 더 많이 발생한다는 것을 알 수 있었다. 한편, 저항성 품종들은 감수성 품종들과 달리 실험한 모든 온도에서 검은썩음병이 발생하지 않았다(Fig. 5).
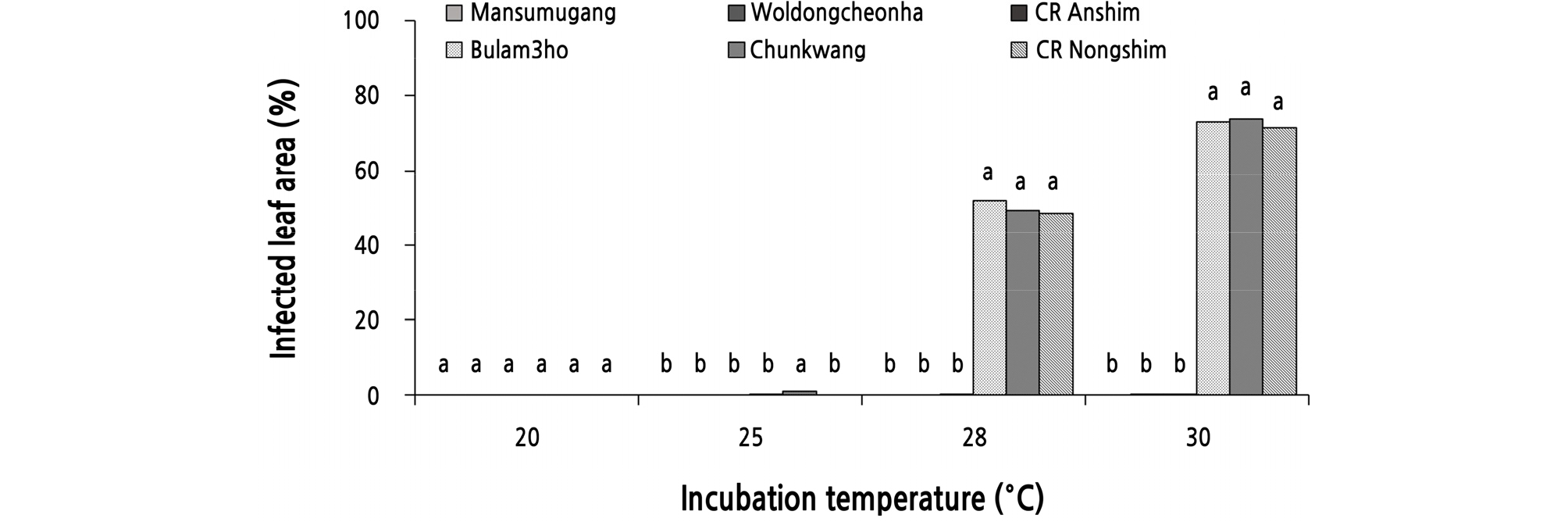
Fig. 5.
Development of black rot on six cultivars of Chinese cabbage according to incubation temperature after inoculation. Ten-day-old seedlings of each cultivar were inoculated with a bacterial suspension (1.0 × 108 cfu/mL) of Xanthomonas campestris pv. campestris KACC 10377 by spray method. The inoculated plants were incubated in a dew chamber at 20, 25, 28, and 30°C for 48 hour and then transferred to a growth room at 25°C and 80% RH with 12-hour light a day. Six days after inoculation, disease severity was measured and represented as percentage of infected leaf area. The data were obtained from ten replicates with two repetitions.Values labeled with the same letter within each incubation temperature are not significantly different based on Duncan’s multiple range test at p = 0.05.
Lee et al.(2013)은 핀셋(mouth-tooth forceps) 접종법으로 검은썩음병균을 양배추 품종들에 접종하고 22, 26, 30°C에서 검은썩음병 발생을 비교하였을 때, 접종 후 22°C에서 재배했을 때 저항성과 감수성 양배추 품종에서 가장 뚜렷한 저항성 차이를 나타냈다고 보고하였다. 그리고 Staub and Williams(1972)도 양배추의 검은썩음병 발생을 16, 20, 24, 28°C에서 실험하였을 때 20 ‑ 24°C에서는 양배추 품종의 저항성이 잘 나타났으나, 28°C에서는 저항성과 감수성 품종 모두 검은썩음병이 많이 발생했다고 보고하였다. 따라서 같은 검은썩음병균에 대한 저항성도 작물에 따라 저항성을 발현하는 적정 온도 그리고 저항성과 감수성 품종의 검은썩음병 발생 차이가 가장 큰 온도는 다르다는 것을 알 수 있었다. 그리고 이와 같은 결과는 작물의 차이에서 기인한 것일 뿐만 아니라 Xcc를 접종하는 방법에 의한 차이일 가능성도 배제할 수 없다. Lee et al.(2013)은 검은썩음병균을 접종할 때 핀셋(mouth-tooth forceps) 접종법을 사용하였고, 본 연구에서는 분무(spray) 접종법으로 Xcc를 접종하였다.
각 품종들의 검은썩음병 발생을 살펴보면, 접종 후에 20°C와 25°C에서 습실처리하였을 때에는 실험한 모든 품종에서 검은썩음병이 발생하지 않았으나, 28°C에서 습실처리하였을 때에는 ‘만수무강’, ‘월동천하’, ‘CR안심’, ‘불암3호’, ‘춘광’, ‘CR농심’은 각각 0, 0, 0.3, 51.9, 49.4, 48.6%의 병반면적률을 보였으며, 접종 후 30°C에서 습실처리하였을 때에는 각 품종들의 병반면적률(%)은 각각 0.0, 0.3, 0.3, 73.0, 73.8, 71.5%이었다(Fig. 5). 따라서 Xcc를 접종하고 28°C와 30°C에서 습실처리하는 것은 둘 다 저항성 품종과 감수성 품종 간에 통계적으로 유의성 있는 차이를 보이나, 30°C에서 습실처리하였을 때 저항성 품종과 감수성 품종의 병반면적률 차이가 가장 크게 나타났으므로, 배추 품종의 저항성을 검정하기 위해서는 배추 유묘에 Xcc를 접종하고 30°C에서 습실처리하는 것이 효과적이라고 생각되었다(Fig. 5).
이상의 결과로부터 검은썩음병균에 대한 배추의 저항성을 검정하기 위해서는, 배추 종자를파종하고 온실(25 ± 5°C)에서 10일 동안 재배하여 2엽이 전개된 배추 유묘에, 접종원의 농도가 1.0 × 108cfu/mL(OD600 = 0.1757)이 되도록 조정한 Xcc 세균현탁액을 spray로 배추 잎의 앞면과 뒷면 모두에 분무접종을 하고, 30°C 습실상에서 48시간 습실처리한 후에 항온항습실(25°C, 상대습도 80%)로 이동하여 하루에 12시간씩 광을 조사하면서 재배하고 감수성 대조 품종에서 검은썩음병이 충분하게 발생하면 병반면적률(%)을 조사하는 것이 효율적이라고 생각된다.





